Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O được Trường TCSP Mẫu giáo – Nhà trẻ Hà Nội biên soạn hướng dẫn bạn đọc viết và cân bằng phương trình phản ứng oxi hóa khử Mg tác dụng HNO3 sản phẩm khử sinh ra NH4NO3. Hy vọng với dung nội cân bằng phương trình phản ứng dưới đây, giúp bạn đọc vận dụng tốt vào làm các dạng câu hỏi bài tập liên quan. Mời các bạn tham khảo.
1. Phương trình phản ứng Mg + HNO3 ra NH4NO3
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
2. Cân bằng phản ứng Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Mg0 + HN+5O3 → Mg+2(NO3)2 + N-3H4NO3 + H2O
Bạn đang xem bài: Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
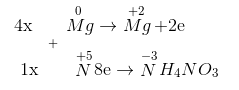
Tỉ lệ 2 muối nitrat của amoni và magiê là 1:4.
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
3. Điều kiện để phản ứng Mg tác dụng HNO3 loãng ra NH4NO3
Nhiệt độ thường
4. Bài tập vận dụng liên quan
Câu 1. Cho phương trình: Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Tổng hệ số cân bằng tối giản của phản ứng trên là
A. 23
B. 24
C. 18
D. 22
Câu 2. Cho Mg tan hoàn toàn trong dung dịch HNO3 loãng không thấy có khí thoát ra . Trong phương trình phản ứng tổng hệ số của các chất (nguyên, tối giản) là bao nhiêu?
A. 20
B. 24
C. 25
D. 22
Câu 3. Cho 4,8 gam Mg tác dụng với dung dịch HNO3 dư. Sau khi phản ứng xảy ra hoàn toàn thu được 1,792 lít NO (đktc) và dung dịch X. Khối lượng muối khan thu được khi cô cạn dung dịch X là
A. 13,92 gam
B. 15,60 gam
C. 16,80 gam
D. 31,20 gam
Ta có:
nMg = 0,2 mol
nNO = 0,08 mol
Các quá trình trao đổi electron
Mg0 → Mg+2 + 2e
0,2 → 0,4
N+5 + 3e→ N+2
0,24 ← 0,08
Vậy còn 1 sản phẩm khử nữa là NH4NO3
N+5 + 8e → N-3
8x → x
Áp dụng bảo toàn electron ta có:
0,4 = 0,24 + 8x → a = 0,02 mol
=> mmuối = mNH4NO3 + mMg(NO3)2 = 31,2 gam
Câu 4. Hòa tan hỗn hợp gồm 2,7 gam Al và 13 gam Zn bằng 500 ml dung dịch HNO3 vừa đủ, thu được dung dịch X và không thấy khí thoát ra. Cô cạn dung dịch X thu a gam muối. Giá trị của a:
A. 66,1 gam
B.
C.
D.
nAl = 2,7/27 = 0,1 mol
nZn = 13/65 = 0,2 mol
Không thấy khí thoát ra => Sản phẩm khử là NH4NO3
⇒ nNH4NO3 = (0,1.3 + 0,2.2)/8 = 0,7/8 mol
Dung dịch muối X gồm: Al(NO3)3 (0,1 mol); Zn(NO3)2 (0,2 mol), NH4NO3 (0,7/8 mol)
m = mAl(NO3)3 + mZn(NO3)2 + mNH4NO3 = 0,1.213 + 0,2.189 + (0,7/8).80 = 66,1 gam
………………………….
Trên đây Trường TCSP Mẫu giáo – Nhà trẻ Hà Nội vừa giới thiệu tới các bạn phương trình phản ứng Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O, mong rằng qua bài viết này các bạn có thể học tập tốt hơn môn Hóa học lớp 11. Mời các bạn cùng tham khảo thêm kiến thức các môn Toán 11, Ngữ văn 11, Tiếng Anh 11, đề thi học kì 1 lớp 11, đề thi học kì 2 lớp 11…
Để tiện trao đổi, chia sẻ kinh nghiệm giảng dạy và học tập môn học THPT, Trường TCSP Mẫu giáo – Nhà trẻ Hà Nội mời các bạn truy cập nhóm riêng dành cho lớp 11 sau: Nhóm Tài liệu học tập lớp 11 để có thể cập nhật được những tài liệu mới nhất.
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục