Axit photphoric là một loại axit có độ bền trung bình, đây cũng là một trong những loại axit rộng rãi và được sử dụng rộng rãi trong thực tiễn cuộc sống.
Đang xem: Đọc H3po4 là gì
Bạn đang xem bài: Axit Photphoric( H3Po4 Đọc Là Gì ? Tính Chất Hóa Học, Cách Điều Chế Và Ứng Dụng
Vì thế Axit photphoric H3PO4 có những tính chất hóa học và vật lý nào? Chúng ta cùng tìm hiểu qua bài viết dưới đây nhé.
* Trong bài học này, học trò cần nắm vững các tính chất hóa học sau của axit photphoric
H3PO4 dễ phân lyPhản ứng với kim loại (trước hydro)Phản ứng với oxit bazơPhản ứng với bazơTác dụng với muốiH3PO4 bị nhiệt phân
Để biết cụ thể về tính chất hóa học của axit photphoric, mời các bạn tham khảo bài viết dưới đây.
I. Tính chất vật lý của axit photphoric H3PO4
– Axit photphoric (H3PO4 ″> H3PO4) Còn được gọi là axit orthophosphoric là một chất rắn kết tinh, trong suốt, ko màu, dễ dàng hòa tan trong nước với bất kỳ tỉ lệ nào.
– Axit photphoric Thường sử dụng là dung dịch đặc, sánh, nồng độ 85% ”> 85%.
Cấu trúc của axit photphoric H3PO4
II. Tính chất hóa học của axit photphoric H3PO4
1. Nó là một axit có độ mạnh trung bình
a) Làm quỳ tím hóa xanh thành đỏ.
Xem thêm: Giá Lan Quế Chi Siêu Rẻ, Trả Hàng Miễn Phí, Bạch Quế Tháng 8
b) Trong dung dịch H3PO4, nó phân ly thuận nghịch theo 3 bước:
H3PO4 ↔ H + + H2PO4-
H2PO4- H + + HPO42-
HPO42- H + + PO43-
c) Phản ứng với oxit bazơ → muối + H2O
2H3PO4 + 3Na2O → 2Na3PO4 + 3H2O
d) Phản ứng với bazơ → muối + H2O (tùy theo vận tốc phản ứng có thể tạo thành các muối không giống nhau).
KOH + H3PO4 → KH2PO4 + H2O
2KOH + H3PO4 → K2HPO4 + 2H2O
3KOH + H3PO4 → K3PO4 + 3H2O
e) Cho kim loại phản ứng với H2 → muối + H2 ↑
2H3PO4 + 3Mg → Mg3 (PO4) 2 + 3H2 ↑
f) Phản ứng với muối → muối mới + axit mới
H3PO4 + 3AgNO3 → 3HNO3 + Ag3PO4
2. Tính oxi hóa – khử
Trong axit photphoric H3PO4 thì P có trạng thái oxi hóa cao nhất +5 nhưng H3PO4 ko có tính oxi hóa như axit nitric HNO3 do nguyên tử P có bán kính lớn hơn N → mật độ điện tích dương trên P nhỏ → khả năng nhận electron kém.
3. Các phản ứng do tác dụng của nhiệt
+ H3PO4 bị nhiệt phân ở 200 – 2500C thành H4P2O7 (Axit điphotphoric)
2H3PO4
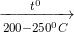
H4P2O7 + H2O
+ Nhiệt phân H4P2O7 ở 400 – 5000C thành HPO3 (Axit photphoric)
H4P2O7

2HPO3 + H2O
Chú ý: Axit photpho H3PO3 là một axit kép.
III. Bài tập về Axit photphoric H3PO4
Bài 4 trang 54 sgk toán 11: Lập các phương trình hóa học sau:
một. H3PO4 + K2HPO4 →
1 mol 1mol
b. H3PO4 + Ca (OH) 2 →
1 mol 1mol
c. 2H3PO4 + Ca (OH) 2 →
2mol 1mol
d. 2H3PO4 + 3Ca (OH) 2 →
2mol 3mol
* Giải bài 4 trang 54 SGK ngữ văn 11: Đây là dạng bài dành cho học trò luyện viết PTPƯ tùy theo tỉ lệ số mol nhưng tạo ra các thành phầm không giống nhau.
một. H3PO4 + K2HPO4 → 2KH2PO4
1 mol 1mol
b. H3PO4 + Ca (OH) 2 → CaHPO4 + 2H2O
1 mol 1mol
c. 2H3PO4 + Ca (OH) 2 → Ca (H2PO4) 2 + 2H2O
2mol 1mol
d. 2H3PO4 + 3Ca (OH) 2 → Ca3 (PO4) 2 + 6H2O
2mol 3mol
Bài 5 trang 54 sgk toán 11: Để thu được một muối photphat trung tính, cần lấy bao nhiêu ml dung dịch NaOH 1,00M để phản ứng với 50,0 ml H3PO4 0,50M?
* Giải bài 5 trang 54 SGK ngữ văn 11:
– Theo đề bài ta có: nH3PO4 = V.CM = 0,05.0,5 = 0,025 (mol).
Xem thêm: Tương khắc là gì, tương khắc là gì & các tuổi tương khắc trong 12 Cung Hoàng Đạo
– Phương trình phản ứng:
H3PO4 + 3NaOH → Na3PO4 + 3H2O
– Từ PTPU suy ra:
nNaOH = 3nH3PO4 = 3. 0,025 = 0,075 (mol)
⇒ VNaOH = n / CM = 0,075 / 1 = 0,075 lít = 75ml
Sự kết luận: Cần 75ml NaOH 1,0M.
Hi vọng với nội dung bài thẩm định về Tính chất hóa học của axit photphoric H3PO4 Trên đây là hữu ích cho các bạn, mọi góp ý và thắc mắc các bạn vui lòng để lại bình luận bên dưới bài viết để được hỗ trợ, chúc các bạn học tốt.
Bạn thấy bài viết Axit Photphoric( H3Po4 Đọc Là Gì ? Tính Chất Hóa Học, Cách Điều Chế Và Ứng Dụng có khắc phục đươc vấn đề bạn tìm hiểu ko?, nếu ko hãy comment góp ý thêm về Axit Photphoric( H3Po4 Đọc Là Gì ? Tính Chất Hóa Học, Cách Điều Chế Và Ứng Dụng bên dưới để tmdl.edu.vn có thể thay đổi & cải thiện nội dung tốt hơn cho độc giả nhé! Cám ơn bạn đã ghé thăm Website Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá
Phân mục: Hỏi đáp
Nguồn: tmdl.edu.vn
Trang chủ: tmdl.edu.vn
Danh mục bài: Tổng hợp