Bài tập về CO2 hay SO2 tác dụng với dung dịch kiềm như NaOH, KOH hay kiềm thổ Ba(OH)2, Ca(OH)2 rất dễ gây bối rối cho nhiều học sinh trong quá trình giải bài tập. Điều này xảy ra đối với cả những em có học lực khá và yêu thích môn hóa học.
Vì vậy mà trong bài viết này, chúng ta cùng hệ thống lại các dạng toán về CO2 hay SO2 tác dụng với dung dịch kiềm như NaOH, KOH, Ba(OH)2 hay Ca(OH)2 và cách giải dạng bài tập này.
Bạn đang xem bài: Các dạng toán CO2, SO2 tác dụng với dung dịch Kiềm NaOH, Ba(OH)2 Phương pháp giải và Bài tập – Hóa 12
° Dạng 1: Bài toán CO2 tác dụng với NaOH, KOH
– Xét phản ứng đặc trưng có thể xảy ra khi cho CO2 tác dụng với dung dịch kiềm NaOH:
CO2 + NaOH → NaHCO3 (1)
PT ion: CO2 + OH– → HCO3–
CO2 + 2NaOH → Na2CO3 (2)
PT ion: CO2 + 2OH– → CO32-
¤ Loại 1: Bài toán cho biết số mol các chất tham gia phản ứng
– Khi bài toán cho biết số mol của NaOH và CO2 tham gia phản ứng:
Bước 1: Lập tỉ lệ mol: 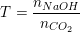
Bước 2: So sánh:
+ Nếu  : chỉ xảy ra phản ứng (1) muối thu được chỉ có NaHCO3
: chỉ xảy ra phản ứng (1) muối thu được chỉ có NaHCO3
+ Nếu 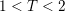 : xảy ra cả phản ứng (1) và (2) sản phẩm thu được gồm 2 muối là NaHCO3 và Na2CO3
: xảy ra cả phản ứng (1) và (2) sản phẩm thu được gồm 2 muối là NaHCO3 và Na2CO3
+ Nếu 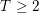 : chỉ xảy ra phản ứng (2) muối thu được chỉ có Na2CO3
: chỉ xảy ra phản ứng (2) muối thu được chỉ có Na2CO3
Bước 3: Tính toán và giải bài toán
* Lưu ý:
– Nếu T<1: Thì CO2 còn dư, NaOH phản ứng hết.
– Nếu 1 ≤ T ≤ 2: Thì CO2 và NaOH đều phản ứng hết.
– Nếu T ≥ 2: Thì CO2 phản ứng hết, NaOH còn dư.
* Ví dụ 1: Dẫn 4,48 lít khí CO2 (ở đktc) qua 250ml dung dịch NaOH 1M. Cô cạn dụng dịch sau phản ứng thu được m gam muối khan. Tính giá trị của m?
° Lời giải:
– Bài cho, 4,48 lít khí CO2 (ở đktc) nên
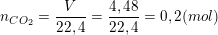
– Bài cho,250ml dung dịch NaOH 1M nên từ
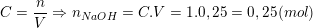
+ Lập tỉ lệ: 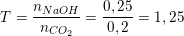
– Ta thấy: 1<T<2 nên tạo ra 2 muối NaHCO3 và Na2CO3
– Gọi x và y lần lượt là số mol của NaHCO3 và Na2CO3
– Ta có các PTPƯ:
CO2 + NaOH → NaHCO3 (1)
x x x (mol)
CO2 + 2NaOH → Na2CO3 (2)
y 2y y (mol)
– Theo bài ra và PTPƯ ta có:
 (*)
(*)
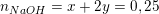 (**)
(**)
– Giải hệ từ (*) và (**) ta được: x=0,15(mol) và y=0,05(mol)
⇒ Khối lượng muối khan thu được:
m(NaHCO3+Na2CO3) = 84.0,15 + 106.0,05 = 17,9(g).
* Ví dụ 2: Cho 5,6 lít CO2 (đktc) đi qua 164ml dung dịch NaOH 20% (d=1,22g/ml) thu được dung dịch X. Cô cạn X thì thu được bao nhiêu gam chất rắn.
° Lời giải:
+ Theo bài ra, ta có:
– bài cho 5,6 lít CO2 (đktc) nên có:
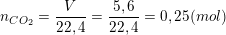
– bài cho 164ml dung dịch NaOH 20% (d=1,22g/ml) nên từ:
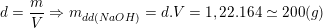
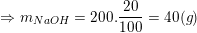
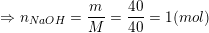
+ Lập tỉ lệ: 
+ So sánh: Ta thấy, T > 2 nên sản phẩm chỉ tạo muối trung hòa Na2CO3,
– Phương trình phản ứng:
CO2 + 2NaOH → Na2CO3
0,25 0,5mol
– Từ phương trình phản ứng, số mol NaOH dư là:
nNaOH (dư) = nNaOH (ban đầu) – nNaOH (pư) = 1 – 0,5 = 0,5(mol).
– Dung dịch X thu được gồm muối Na2CO3 và NaOH dư
⇒ khối lượng chất rắn là:
mcr = mNa2CO3 + mNaOH = 0,25.106 + 0,5.40 = 26,5 + 20 = 46,5(g)
¤ Loại 2: Khi CHƯA biết số mol các chất tham gia phản ứng
– Bài toán chưa cho biết số mol của CO2 và NaOH tham gia phản ứng:
Bước 1: Viết cả hai phương trình phản ứng (1) và (2)
Bước 2: Gọi số mol của mỗi muối tương ứng
Bước 3: Tính toán và giải bài toán
* Ví dụ 1: Hấp thụ hoàn toàn 15,68 lít khí CO2 (đktc) vào 500ml dung dịch NaOH có nồng độ C mol/lít. Sau phản ứng thu được 65,4 gam muối. Tính C.
° Lời giải:
– Theo bài ra, Hấp thụ hoàn toàn 15,68 lít khí CO2 (đktc), ta có:
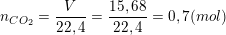
– Gọi số mol của muối NaHCO3 và Na2CO3 lần lượt là x và y
– Ta có PTPƯ:
CO2 + NaOH → NaHCO3 (1)
x x x (mol)
CO2 + 2NaOH → Na2CO3 (2)
y 2y y (mol)
– Theo bài ra và theo PTPƯ ta có:
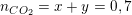 (*)
(*)
– Khối lượng của muối là:
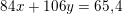 (**)
(**)
– Giải hệ từ (*) và (**) ta được: x = 0,4(mol) và y = 0,3(mol)
– Từ PTPƯ ta có: nNaOH = x + 2y = 0,4 + 2.0,3 = 1(mol)
⇒ Nồng độ của 500 ml (0,5 lít) dd NaOH là: 
° Dạng 2: Bài toán CO2 tác dụng với Ca(OH)2, Ba(OH)2
– Xét phản ứng đặc trưng có thể xảy ra khi cho CO2 tác dụng với dung dịch kiềm thổ Ca(OH)2, Ba(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O (1)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
¤ Loại 1: Bài toán cho biết số mol các chất tham gia phản ứng
– Khi bài toán cho biết số mol của Ca(OH)2 và CO2 tham gia phản ứng:
Bước 1: Lập tỉ lệ: 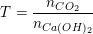
Bước 2: So sánh
+ Nếu  : chỉ xảy ra phản ứng (1) muối thu được chỉ có CaCO3
: chỉ xảy ra phản ứng (1) muối thu được chỉ có CaCO3
+ Nếu 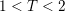 : xảy ra cả phản ứng (1) và (2) sản phẩm thu được gồm 2 muối là Ca(HCO3)2 và CaCO3
: xảy ra cả phản ứng (1) và (2) sản phẩm thu được gồm 2 muối là Ca(HCO3)2 và CaCO3
+ Nếu 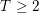 : chỉ xảy ra phản ứng (2) muối thu được chỉ có Ca(HCO3)2
: chỉ xảy ra phản ứng (2) muối thu được chỉ có Ca(HCO3)2
Bước 3: Tính toán và giải bài toán
* Ví dụ 1: Sục 0,336 lít khí CO2 (đktc) vào 1 lít dung dịch Ca(OH)2 0,01M thu được m gam kết tủa. Tìm m?
° Lời giải:
– Theo bài ra, có 0,336 lít khí CO2 (đktc) nên:
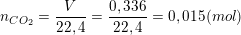
– bài ra, có 1 lít dung dịch Ca(OH)2 0,01M, nên:

+ Lập tỉ lệ và so sánh: 
⇒ Xảy ra cả hai phản ứng
– Gọi x, y lần lượt là số mol CaCO3 và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
x x x (mol)
2CO2 + Ca(OH)2 → Ca(HCO3)2
2y y y (mol)
– Theo bài ra và theo PTPƯ ta có số mol CO2 là:
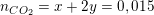 (*)
(*)
– Tương tự, số mol Ca(OH)2 là:
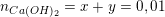 (**)
(**)
– Giải hệ từ (*) và (**) ta được: x = y = 0,005(mol)
⇒ Khối lượng kết tủa CaCO3 là: mCaCO3 = n.M = 0,005.100 = 0,5(g).
¤ Loại 2: Bài toán CHƯA biết số mol các chất tham gia phản ứng
– Với bài toán dạng này, thường cho biết số mol của CO2 hoặc Ca(OH)2 và số mol của CaCO3 khi giải ta viết cả hai phương trình phản ứng và biện luận:
• TH1: Chỉ xảy ra phản ứng tạo kết tủa CaCO3
• TH2: Xảy ra cả hai phản ứng tạo muối trung hòa CaCO3 và muối axit Ca(HCO3)2
* Lưu ý:
– Khi bài toán cho thể tích CO2 và khối lượng kết tủa CaCO3 yêu cầu tính khối lượng kiềm thì thường chỉ xảy ra 1 trường hợp và có 1 đáp án phù hợp.
– Khi bài toán cho khối lượng kiềm và khối lượng chất kết tủa CaCO3 yêu cầu tính thể tích khí CO2 thì thường xảy ra 2 trường hợp và có 2 kết quả thể tích CO2 phù hợp.
* Ví dụ 1: Hấp thụ toàn bộ 2,688 lít CO2 (đktc) vào 2,5 lít dung dịch Ba(OH)2 b mol/l thu được 15,76 gam kết tủa. Tính b.
° Lời giải:
– Theo bài ra, số mol khí CO2 là:

– Kết tủa là BaCO3 nên số mol kết tủa thu được là:
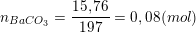
– Ta thấy: 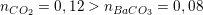 nên xảy ra hai phản ứng
nên xảy ra hai phản ứng
– Ta có các PTPƯ như sau
CO2 + Ba(OH)2 → BaCO3↓ + H2O (1)
0,08 0,08 0,08 (mol)
2CO2 + Ba(OH)2 → Ba(HCO3)2 (2)
0,04 0,02 0,02 (mol)
– Theo PTPƯ (1) ta có
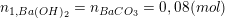
– Số mol CO2 còn lại sau phản ứng (1) sẽ tham gia phản ứng (2) là:
nCO2(pư (2)) = 0,12 – 0,08 = 0,04(mol)
– Và theo PTPƯ (2) ta có:
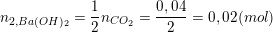
⇒ Tổng số mol Ba(OH)2 tham gia phản ứng là: nBa(OH)2 = 0,08 + 0,02 = 0,1(mol).
⇒ 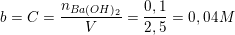
° Dạng 3: Bài toán CO2 tác dụng với dd kiềm, kiềm thổ: NaOH, Ca(OH)2
– Đối với dạng bài toán này, nên sử dụng phương trình ion để giải bài toán:
CO2 + OH– → HCO3– (1)
CO2 + 2OH– → CO32- + H2O (2)
Ca2+ + CO32- → CaCO3↓ (3)
¤ Loại 1: Bài toán cho biết số mol các chất tham gia phản ứng
– Khi bài toán cho biết số mol của CO2, NaOH và Ca(OH)2 ta thực hiện:
Bước 1: Lập tỉ số: 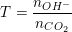
Bước 2: So sánh
+ Nếu  : chỉ xảy ra phản ứng (1) tạo muối HCO3–
: chỉ xảy ra phản ứng (1) tạo muối HCO3–
+ Nếu 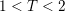 : xảy ra cả phản ứng (1) và (2) tạo 2 muối HCO3– và CO32-
: xảy ra cả phản ứng (1) và (2) tạo 2 muối HCO3– và CO32-
+ Nếu 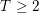 : chỉ xảy ra phản ứng (2) tạo muối CO32-
: chỉ xảy ra phản ứng (2) tạo muối CO32-
Bước 3: Tính toán và giải bài toán
* Ví dụ 1: Hấp thụ hoàn toàn 4,48 lít khí CO2 (đktc) vào 500ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,2M sinh ra m gam kết tủa. Tìm m?
° Lời giải:
– Theo bài ra, ta có số mol CO2 , NaOH và Ba(OH)2 là:


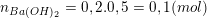
* Lưu ý: NaOH → Na+ + OH– và Ba(OH)2 → Ba2+ + 2.OH–
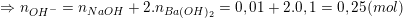
+ Lập tỉ lệ: 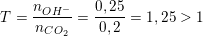 nên tạo 2 muối
nên tạo 2 muối
– Ta có các PTPƯ:
CO2 + OH– → HCO3– (1)
x x x (mol)
CO2 + 2OH– → CO32- + H2O (2)
y 2y y (mol)
Ba2+ + CO32- → BaCO3↓ (3)
y y y (mol)
– Từ PTPƯ (1) và (2) ta có:
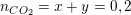
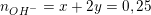
– Từ 2 phương trình trên giải hệ ta được: x = 0,15(mol); y =0,05(mol)
– Từ PTPƯ (3) ta có: 
– Khối lượng kết tủa là: 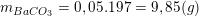
¤ Loại 2: Bài toán CHƯA cho biết số mol các chất tham gia phản ứng
– Với bài toán loại này thường cho biết số mol của CO2 hoặc của kiềm NaOH và số mol kết tủa CaCO3 khi giải phải viết ba phương trình phản ứng và biện luận:
• TH1: OH– dư, chỉ xảy ra phản ứng (2) và (3) khi đó: 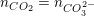
• TH2: OH– và CO2 đều hết, xảy ra cả ba phản ứng (1), (2), (3) khi đó: 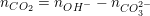
* Lưu ý:
– Khi tính kết tủa phải so sánh số mol CO32- với Ca2+ hay Ba2+ rồi mới kết luận số mol kết tủa:
+ Nếu 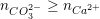 thì n↓ = nCa2+
thì n↓ = nCa2+
+ Nếu  thì n↓ = nCO32-
thì n↓ = nCO32-
* Ví dụ 1: Sục V lít khí CO2 (ở đktc) vào 200ml dung dịch X gồm Ba(OH)2 1M và NaOH 1M. Sau phản ứng thu được 19,7 gam kết tủa. Tính giá trị của V?
° Lời giải:
– Theo bài ra, ta có số mol của Ba(OH)2 và NaOH, BaCO3 là:
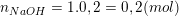
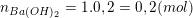
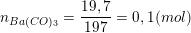
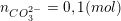
+ Lưu ý: NaOH → Na+ + OH– và Ba(OH)2 → Ba2+ + 2OH– nên
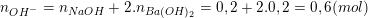
+ TH1: OH– dư, CO2 hết:
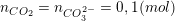
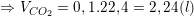
+ TH2: OH– hết và CO2 cũng hết:
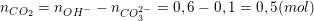
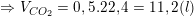
* Ví dụ 2: Hấp thụ hoàn toàn V lít khí CO2 (ở đktc) vào 100ml dung dịch hỗn hợp gồm KOH 1M và Ca(OH)2 0,25M sinh ra 2,5gam kết tủa. Tìm V?
° Lời giải:
– Theo bài ra, ta có số mol KOH, Ca(OH)2 và CaCO3 kết tủa là:
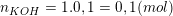
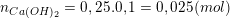

– Ta có: 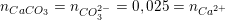 nên OH– và CO2 đều hết
nên OH– và CO2 đều hết
+ Lưu ý: KOH → K+ + OH– và Ca(OH)2 → Ca2+ + 2OH– nên

– Số mol CO2 là: 
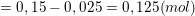
⇒ Thể tích khí CO2 là: 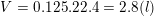
Hy vọng với bài viết về Các dạng toán CO2, SO2 tác dụng với dung dịch Kiềm NaOH, Ba(OH)2 Phương pháp giải và Bài tập ở trên hữu ích cho các em. Mọi góp ý và thắc mắc các em vui lòng để lại bình luận dưới bài viết để HayHocHoi.Vn ghi nhận và hỗ trợ, chúc các em học tập tốt.
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn/cac-dang-toan-co2-so2-tac-dung-voi-dung-dich-kiem-naoh-baoh2-phuong-phap-giai-va-bai-tap-hoa-12/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục