Hóa 11 bài 44: Tính chất hóa học của Andehit – Xeton, công thức cấu tạo và bài tập vận dụng. Andehit và Xeton đều là những hợp chất hữu cơ mà trong phân tử có chứa nhóm chức, đối với Andehit là nhóm -CH=O còn Xeton là nhóm -C=O- liên kết trực tiếp với 2 gốc hidro cacbon.
Vậy Andehit và Xeton có công thức cấu tạo cụ thể như thế nào, tính chất hóa học của andehit và xeton có gì khác với các hidrocacbon khác. Chúng đươc ứng dụng vào lĩnh vực gì và cách điều chế Andehit – Xeton như thế nào? chúng ta hãy cùng tìm hiểu chi tiết qua bài viết dưới đây.
Bạn đang xem bài: Hóa 11 bài 44: Tính chất hóa học của Andehit – Xeton, công thức cấu tạo và bài tập vận dụng
A. ANDEHIT
I. Andehit – Định nghĩa, phân loại và danh pháp
1. Andehit là gì?
– Định nghĩa: Anđehit là hợp chất hữu cơ mà phân tử có nhóm -CH=O liên kết với gốc hiđrocacbon, với H hoặc với nhau.
– Công thức cấu tạo andehit: 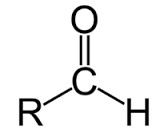
– Nhóm -CH=O là nhóm chức andehit
Ví dụ: H-CH=O andehit fomic hoặc metanal
CH3-CH=O andehit axetic hoặc etanal
C6H5-CH=O benzandehit
O=CH-CH=O andehit oxalic
– Công thức tổng quát của anđehit:
• CxHyOz (x, y, z là các số nguyên dương; y chẵn; 2 ≤ y ≤ 2x + 2 – 2z; z ≤ x): thường dùng khi viết phản ứng cháy.
• CxHy(CHO)z hay R(CHO)z: thường dùng khi viết phản ứng xảy ra ở nhóm CHO.
• CnH2n+2-2k-z(CHO)z (k = số liên kết p + số vòng): thường dùng khi viết phản ứng cộng H2, cộng Br2,…
2. Phân loại andehit
– Dựa theo cấu tạo của gốc hiđrocacbon, người ta phân chia anđehit và xeton thành ba loại: no, không no và thơm.
Ví dụ: CH3-CH=O thuộc loại anđehit no,
CH2=CH-CH=O thuộc loại anđehit không no,
C6H5-CH=O thuộc loại anđehit thơm,
CH2-CO-CH3 thuộc loại xeton no,
CH3-CO-C6H5 thuộc loại xeton thơm,…
3. Danh pháp – Cách gọi tên andehit
a) Tên thay thế
– Tên thay thế = Tên hiđrocacbon tương ứng + al
b) Tên thường
– Tên thường = Anđehit + Tên axit tương ứng
Tên axit (thay hậu tố “ic” bằng “anđehit”)
* Chú ý: Dung dịch HCHO 37% → 40% gọi là: Fomalin hay fomon.
II. Tính chất vật lý, tính chất hóa học, điều chế và ứng dụng Andehit
1. Tính chất vật lý của andehit
– Chỉ có HCHO, CH3CHO là chất khí. Các anđehit còn lại đều là chất lỏng.
– Anđehit có nhiệt độ sôi thấp hơn Ancol có khối lượng phân tử tương đương nhưng cao hơn so với hidrocacbon có cùng số nguyên tử C trong phân tử.
2. Tính chất hóa học của andehit
a) Andehit tác dụng với hiđro (andehit + H2)
R(CHO)x + xH2 ![small dpi{100} fn_cm small dpi{100} fn_cm small xrightarrow[]{Ni,t^{0}} 1552443703fsrw2isgc0](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443703fsrw2isgc0.gif) R(CH2OH)x
R(CH2OH)x
* Chú ý: Trong phản ứng của anđehit với H2: Nếu gốc R có các liên kết pi thì H2 cộng vào cả các liên kết pi đó. Phản ứng với H2 chứng tỏ anđehit có tính oxi hóa.
b) Andehit tác dụng với AgNO3/NH3 (gọi là phản ứng tráng bạc)
R(CHO)x + 2xAgNO3 + 3xNH3 + xH2O → R(COONH4)x + xNH4NO3 + 2xAg
– Phản ứng chứng minh anđehit có tính khử và được dùng để nhận biết anđehit.
– Riêng HCHO có phản ứng:
HCHO + 4AgNO3 + 6NH3 + 2H2O → (NH4)2CO3 + 4NH4NO3 + 4Ag
* Chú ý: Phản ứng tổng quát ở trên áp dụng với anđehit không có nối ba nằm đầu mạch. Nếu có nối ba nằm ở đầu mạch thì H của C nối ba cũng bị thay thế bằng Ag.
– Các đặc điểm của phản ứng tráng gương của anđehit:
+ Nếu nAg = 2nanđehit → anđehit thuộc loại đơn chức và không phải HCHO.
+ Nếu nAg = 4nanđehit → anđehit đó thuộc loại 2 chức hoặc HCHO.
+ Nếu nAg > 2nhỗn hợp các anđehit đơn chức thì hỗn hợp đó có HCHO.
+ Số nhóm CHO = nAg/2nanđehit (nếu trong hỗn hợp không có HCHO).
– Một số loại chất khác cũng có khả năng tham gia phản ứng tráng gương gồm:
+ HCOOH và muối hoặc este của nó: HCOONa, HCOONH4, (HCOO)nR. Các chất HCHO, HCOOH, HCOONH4 khi phản ứng chỉ tạo ra các chất vô cơ.
+ Các tạp chức có chứa nhóm chức CHO: glucozơ, fructozơ, mantozơ…
c) Andehit có phản ứng oxi hóa (andehit + O2)
* Oxi hóa hoàn toàn
CxHyOz + (x + y/4 – z/2)O2 → xCO2 + y/2H2O
– Nếu đốt cháy anđehit mà nCO2 = nH2O thì anđehit thuộc loại no, đơn chức, mạch hở.
CnH2n+1CHO → (n + 1)CO2 + (n + 1)H2O
* Phản ứng oxi hóa không hoàn toàn
R(CHO)x + x/2O2 ![small dpi{100} fn_cm small dpi{100} fn_cm small xrightarrow[]{Mn^{2+},t^{0}} 1552443706gbdjg2ho6c](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443706gbdjg2ho6c.gif) R(COOH)x
R(COOH)x
– Đối với bài toán oxi hóa anđehit thành axit cần chú ý định luật bảo toàn khối lượng trong quá trình giải.
d) Phản ứng với Cu(OH)2 ở nhiệt độ cao (andehit + Cu(OH)2)
R(CHO)x + 2xCu(OH)2↓ xanh → R(COOH)x + xCu2O↓ đỏ gạch + 2xH2O
→ Phản ứng này được dùng để nhận biết anđehit.
* Chú ý: Phản ứng với Cu(OH)2 thường được thực hiện trong môi trường kiềm nên có thể viết phản ứng dưới dạng:
R(CHO)x + 2xCu(OH)2 + xNaOH → R(COONa)x + xCu2O + 3xH2O
HCOOH, HCOOR, HCOOM, glucozơ, fructozơ, mantozơ cũng có phản ứng này.
e) Phản ứng với dung dịch Br2 (andehit + Br2)
R(CHO)x + xBr2 + xH2O → R(COOH)x + 2xHBr
– Nếu anđehit còn có liên kết pi ở gốc hiđrocacbon thì xảy ra đồng thời phản ứng cộng Br2 vào liên kết pi đó.
3. Điều chế andehit
a) Oxi hóa ancol bậc I
R(CH2OH)x + xCuO ![small dpi{100} fn_cm small dpi{100} fn_cm small xrightarrow[]{t^{0}} 15524437195spw7vljvm](https://tmdl.edu.vn/wp-content/uploads/2023/03/15524437195spw7vljvm.gif) R(CHO)x + xCu + xH2O
R(CHO)x + xCu + xH2O
b) Điều chế qua ancol không bền
– Cộng H2O vào C2H2:
C2H2 + H2O ![small dpi{100} fn_cm small dpi{100} fn_cm small xrightarrow[]{H_{2}SO_{4},HgSO_{4},80^{0}C} 15524437236sotfh6m8e](https://tmdl.edu.vn/wp-content/uploads/2023/03/15524437236sotfh6m8e.gif) CH3CHO
CH3CHO
– Thủy phân este của ancol không bền thích hợp (andehit + NaOH)
CH3COOCH=CH2 + NaOH → CH3COONa + CH3CHO
– Thủy phân dẫn xuất 1,1-đihalogen:
CH3-CHCl2 + 2NaOH → CH3CHO + 2NaCl + H2O
c) Một số phản ứng đặc biệt
2CH3OH + O2 ![small xrightarrow[]{Ag,600^{0}C} 1552443727rwo5z4rb5i](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443727rwo5z4rb5i.gif) 2HCHO + 2H2O
2HCHO + 2H2O
CH4 + O2 ![small dpi{100} fn_cm small xrightarrow[]{xt,t^{0}} 1552443731h16q0hkzau](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443731h16q0hkzau.gif) HCHO + H2O
HCHO + H2O
2CH2=CH2 + O2 ![small dpi{100} fn_cm small dpi{100} fn_cm small xrightarrow[]{PdCl_{2},CuCl_{2}}](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443734hzw7ro0x1p.gif) 2CH3CHO
2CH3CHO
4. Nhận biết Anđehit
– Tạo kết tủa sáng bóng với AgNO3/NH3.
– Tạo kết tủa đỏ gạch với Cu(OH)2 ở nhiệt độ cao.
– Làm mất màu dung dịch nước Brom.
(Riêng HCHO phản ứng với dung dịch Brom có khí CO2 thoát ra).
5. Ứng dụng của Andehit
– Fomandehit được dùng chủ yếu để sản xuất poliphenolfomandehit (làm chất dẻo), dùng trong tổng hợp phẩm nhuộm, dược phẩm.
– Dung dịch 37 – 40% của fomandehit trong nước gọi là fomon hay fomalin dùng để ngâm xác động vật, thuộc da, tẩy uế, diệt trùng…
– Axetandehit được dùng chủ yếu để sản xuất axit axetic.
B. XETON
I. Xeton – định nghĩa, danh pháp
1. Xeton là gì?
– Định nghĩa: Xeton là hợp chất hữu cơ mà phân tử có nhóm chức -C(=O)- liên kết trực tiếp với 2 nguyên tử C.
– Công thức cấu tạo của xeton: 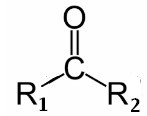
– Công thức tổng quát của xeton đơn chức có dạng: R1-CO-R2
Ví dụ: CH3-CO-CH3 dimetyl xeton (axeton)
CH3-CO-C6H5 metyl phenyl xeton (axelophenon)
CH3-CO-CH=CH2 metyl vinyl xeton
2. Danh pháp – cách gọi tên xeton
a) Tên thay thế
– Tên thay thế = Tên hidrocacbon + số chỉ vị trí C trong nhóm CO + on
b) Tên gốc – chức
– Tên gốc chức = Tên gốc R1 , R2 + xeton
Ví dụ: CH3-CO-CH3 dimetyl xeton (axeton)
CH3-CO-C6H5 metyl phenyl xeton (axelophenon)
II. Tính chất hóa học, ứng dụng và điều chế Xeton
1. Tính chất hóa học của Xeton
a) Phản ứng với H2/Ni, t0 tạo ancol bậc II: (Xeton + H2)
R1-CO-R2 + H2 ![small xrightarrow[]{Ni,t^{0}} 15524437375y73wznomb](https://tmdl.edu.vn/wp-content/uploads/2023/03/15524437375y73wznomb.gif) R1-CHOH-R2
R1-CHOH-R2
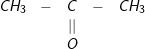 + H2
+ H2 ![small xrightarrow[]{Ni,t^{0}} 15524437375y73wznomb](https://tmdl.edu.vn/wp-content/uploads/2023/03/15524437375y73wznomb.gif)
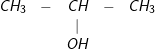
– Xeton không có phản ứng tráng gương, không phản ứng với Cu(OH)2 ở nhiệt độ cao, không làm mất màu dung dịch Brom như anđehit.
b) Phản ứng thế ở gốc hidrocacbon vị trí bên cạnh nhóm CO: (Xeton + Br2)
CH3COCH3 + Br2 → CH3COCH2Br + HBr (có CH3COOH)
2. Điều chế Xeton
– Cho ancol bậc II + CuO đun nóng:
RCHOHR’ + CuO ![small xrightarrow[]{t^{0}} 1552443750ihz0c11buh](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443750ihz0c11buh.gif) RCOR’ + Cu + H2O
RCOR’ + Cu + H2O
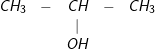 + CuO
+ CuO ![small xrightarrow[]{t^{0}} 1552443750ihz0c11buh](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443750ihz0c11buh.gif) CH3-CO-CH3 + H2O + Cu
CH3-CO-CH3 + H2O + Cu
– Điều chế gián tiếp qua ancol không bền:
CH3COOC(CH3) = CH2 + NaOH → CH3COONa + CH3COCH3
– Oxi hóa cumen (C6H5CH(CH3)2) để sản xuất axeton.
3. Ứng dụng của Xeton
– Axeton được dùng làm dung môi trong sản xuất nhiều hóa chất.
– Axeton còn là chất đầu để tổng hợp nhiều chất hữu cơ quan trọng khác.
C. Bài tập Andehit – Xeton
Bài 1 trang 203 SGK Hóa 11: Thế nào là anđehit? Viết công thức cấu tạo của các anđehit có công thức phân tử C4H8O và gọi tên chúng.
* Lời giải bài 1 trang 203 SGK Hóa 11:
– Trong Công thức phân tử C4H8O phải có nhóm chức andehit -CH=O, nhóm chức này liên kết trực tiếp với nguyên tử cacbon(1) hoặc nguyên tử hiđro.
– CTCT của anđehit có công thức phân tử C4H8O là:
CH3-CH2-CH2-CHO : Butanal
hoặc 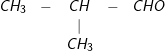 : 2 – metylpropanal
: 2 – metylpropanal
Bài 3 trang 203 SGK Hóa 11: Hoàn thành dãy chuyển hóa sau bằng các phương trình hóa hoc:
Metan → metyl clorua → metanol → metanal → axit fomic
* Lời giải bài 3 trang 203 SGK Hóa 11:
– Phương trình hóa học của dãy chuyển hóa:
CH4 + Cl2 ![small xrightarrow[]{as',1:1} 1552443762fd50d46yd0](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443762fd50d46yd0.gif) CH3Cl + HCl
CH3Cl + HCl
CH3Cl + NaOH ![small xrightarrow[]{t^{0}} 1552443750ihz0c11buh](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443750ihz0c11buh.gif) CH3OH + NaCl
CH3OH + NaCl
CH3OH + CuO ![small xrightarrow[]{t^{0}} 1552443750ihz0c11buh](https://tmdl.edu.vn/wp-content/uploads/2023/03/1552443750ihz0c11buh.gif) HCHO + Cu + H2O
HCHO + Cu + H2O
2HCHO + O2 ![small dpi{100} fn_cm small xrightarrow[]{t^{0},xt}](https://tmdl.edu.vn/wp-content/uploads/2023/03/155244377102ls6nxgd7.gif) 2HCOOH
2HCOOH
Bài 4 trang 203 SGK Hóa 11: Cho 1,0 ml dung dịch fomanđehit 5% và 1,0 ml dung dịch NaOH 10,0% vào ống nghiệm, sau đó thêm tiếp từng giọt dung dịch CuSO4và lắc đều cho đến khi xuất hiện kết tuả. Đun nóng phần dung dịch phía trên, thấy có kết tủa màu đỏ gạch của Cu2O. Giải thích hiện tượng thí nghiệm và viết phương trình hóa học.
* Lời giải Bài 4 trang 203 SGK Hóa 11:
– Khi nhỏ dung dịch CuSO4 vào thì có kết tủa xanh xuất hiện:
2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO4
– Khi đun nóng phần trên ống nghiệm trên ngọn lửa đèn cồn thì có kết tủa đỏ gạch xuất hiện:
HCHO + 4Cu(OH)2 + 2NaOH → Na2CO3 + 2 Cu2O↓đỏ gạch + 6H2O
Bài 5 trang 203 SGK Hóa 11: Cho 50,0 gam dung dịch anđehit axetic tác dụng với dung dịch AgNO3 trong NH3 (đủ) thu được 21,6 gam Ag kết tủa. Tính nồng đồ % của anđehit axetic trong dung dịch đã dùng.
* Lời giải Bài 5 trang 203 SGK Hóa 11:
– Phương trình phản ứng
CH3CHO + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3
– Theo bài ra, ta có: nAg = m/M = 21,6/108 = 0,2 (mol).
– Theo PTPƯ ta có: nCH3CHO = ½nAg = ½.0,2 = 0,1 (mol).
⇒ C%CH3CHO = 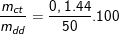 % = 8,8%
% = 8,8%
Bài 7 trang 203 SGK Hóa 11: Cho 8,0 gam hỗn hợp hai anđehit kế tiếp nhau trong dãy đồng đẳng của anđehit no, đơn chức, mạch hở tác dụng với bạc nitrat trong dung dịch ammoniac (lấy dư) thu được 32,4 gam bạc kết tủa. Xác định công thức phân tử, viết công thức cấu tạo và gọi tên các anđehit.
*Lời giải bài 7 trang 203 SGK Hóa 11:
– Gọi công thức chung của anđehit là: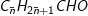 (n≥0)
(n≥0)
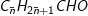 + 2AgNO3 + 3NH3 →
+ 2AgNO3 + 3NH3 → 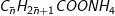 + 2Ag + 2NH4NO3
+ 2Ag + 2NH4NO3
– Theo bài ra, ta có: nAg = 32,4/108 = 0,3 (mol).
– Theo PTPƯ, ta có: 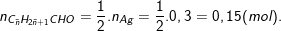
⇒ Khối lượng trung bình của andehit: 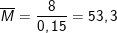
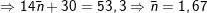 (vậy n=1 và n = 2)
(vậy n=1 và n = 2)
⇒ 2 anđehit kế tiếp nhau là : CH3CHO (etanal) và C2H5CHO (etanal)
Bài 8 trang 204 SGK Hóa 11: Oxi hóa không hoàn toàn etilen (có xúc tác) để điều chế anđehit axetic thu được hỗn hợp X. Dẫn 2,24 lít khí X (quy về đktc) vào một lượng dư dung dịch bạc nitrat trong NH3 đến khi phản ứng hoàn toàn thấy có 16,2 gam bạc kết tủa.
a. Viết phương trình hóa học của các phản ứng xảy ra.
b. Tính hiệu suất của quá trình oxi hóa etilen.
* Lời giải bài 8 trang 204 SGK Hóa 11:
– Phương trình phản ứng:
2CH2=CH2 + O2 → 2CH3CHO (1)
– Hỗn hợp X gồm: CH2=CH2 và CH3CHO
CH3CHO + H2O + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3 (2)
– Theo bài ra, ta có: 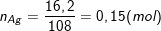 và
và 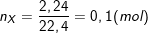
– Theo PTPƯ (2): nCH3CHO = (1/2)nAg = (1/2).0,15 = 0,075 (mol).
⇒ nCH2=CH2 (pư) = nCH3CHO = 0,075 (mol).
⇒ nCH2=CH2 (trong X) = nX – nCH3CHO = 0,1 – 0,075 = 0,025 (mol).
⇒ Hiệu suất của phản ứng: 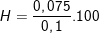 % = 75%
% = 75%
Bài 9 trang 204 SGK Hóa 11: Hợp chất X no, mạch hở có phần trăm khối lượng C và H lần lượt bằng 66,67% và 11,11% còn lại là O. tỉ số hơi của X so với oxi bằng 2,25
a. Tìm công thức phân tử của X
b. X không tác dụng với dung dịch AgNO3 trong NH3 nhưng khi tác dụng với hidro sinh ra X1. X1 tác dụng được với natri giải phóng hidro. Viết công thức cấu tạo va gọi tên của hợp chất X?
* Lời giải bài 9 trang 204 SGK Hóa 11:
a) Theo bài ra, ta có: %O = 100% – %C – %H = 100% – 66,67% – 11,11% = 22,22%
– Mặt khác: dx/O2 = (Mx/32) = 2,25 ⇒ MX = 2,25.32 = 72 (g).
– Gọi công thức phân tử của X là CxHyOz
– Ta có tỉ số: 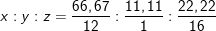
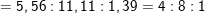
⇒ Công thức đơn giản nhất của X là C4H8O
– Gọi công thức phân tử của X là (C4H8O)n
⇒ MX = (4.12 + 8 + 16)n = 72n = 72 ⇒ n = 1
⇒ Công thức phân tử của X là C4H8O
b) X không tác dụng được với dung dịch AgNO3 trong NH3, khi tác dụng với hiđro sinh ra X1, X1 tác dụng natri giải phóng hiđro ⇒ X là xeton
– CTCT và tên gọi của X là: 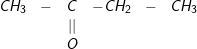 : Etyl metyl xeton
: Etyl metyl xeton
Hy vọng với bài viết về tính chất hóa học, công thức cấu tạo của Andehit, Xeton và bài tập vận dụng ở trên giúp các em hiểu rõ về andehit – xeton cách điều chế và ứng dụng các hợp chất này. Mọi thắc mắc và góp ý các em vui lòng để lại bình luận dưới bài viết để Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá ghi nhận và hỗ trợ, chúc các em học tập tốt!
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn/hoa-11-bai-44/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục





