Hoá 12 bài 1: Tính chất hoá học của Este, bài tập về Este. Este được ứng dụng nhiều trong thực tế như một số este dùng là chất hóa dẻo, dược phẩm; một số khác có mùi thơm hoa quả được dùng trong công nghiệp thực phẩm và mĩ phẩm,…
Vậy Este là gì? Este có những tính chất hoá học và tính chất vật lý nào? chúng ta cùng tìm hiểu qua bài viết dưới đây để hiểu rõ hơn nhé các em.
Bạn đang xem bài: Hoá 12 bài 1: Tính chất hoá học của Este, bài tập về Este
I. Este là gì?
– Este là sản phẩm thu được khi thay thế nhóm OH trong axit cacboxylic bằng nhóm OR.
– Este đơn giản có công thức cấu tạo như sau: 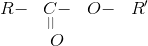
– Công thức tổng quát của một số loại este thường gặp:
+ Este no, đơn chức, mạch hở: CnH2n+1COOCmH2m+1 hay CxH2xO2 (n ≥ 0; m ≥ 1; x ≥ 2).
+ Este đơn chức: CxHyO2 hoặc RCOOR’ (x ≥ 2; y ≥ 4; y chẵn; y ≤ 2x):
+ Este của axit đơn chức và Ancol đa chức: (RCOO)xR’.
+ Este của axit đa chức và Ancol đơn chức: R(COOR’)x.
+ Este của axit đa chức và Ancol đa chức: Rt(COO)xyR’x.

* Lưu ý: Số chức este là bội số chung nhỏ nhất của số chức ancol và số chức axit.
II. Cách đọc tên Este (danh pháp).
1. Với ancol đơn chức R’OH
Tên este = tên gốc hidrocacbon R’+ tên gốc axit (đổi đuôi ic thành at )
Ví dụ: HCOOC2H5 : Etyl fomat;
CH3COOC2H5: Etyl axetat
CH2=CH-COO-CH3: Metyl acrylat
2. Với ancol đa chức
Tên este = tên ancol + tên gốc axit
Ví dụ: CH2OOC-CH3: etylenglycol điaxetat
III. Tính chất vật lý của Este
– Đa số ở trạng thái lỏng, những este có khối lượng phân tử rất lớn có thể ở trạng thái rắn (như mỡ động vật, sáp ong,…)
– Nhiệt độ sôi thấp, dễ bay hơi do không tạo liên kết hidro giữa các phân tử.
– Nhẹ hơn nước, ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử với nước.
– Đa số các este có mùi thơm đặc trưng như:
- Isoamyl axetat: CH3COOCH2CH2(CH3)2 có mùi chuối
- Etyl butirat: CH3CH2CH2COOC4H9 có mùi dứa
- Geranyl axetat: CH3COOC10H17 có mùi hoa hồng
– Là dung môi tốt để hòa tan các chất hữu cơ.
IV. Tính chất hoá học của Este
1. Este phản ứng thủy phân
RCOOR’ + H2O ↔ RCOOH + R’OH
– Phản ứng thực hiện trong môi trường axit loãng và được đun nóng.
– Muốn tăng hiệu suất của phản ứng thủy phân este phải dùng dư nước và sử dụng chất xúc tác axit, đun nóng hỗn hợp phản ứng.
– Nếu ancol sinh ra không bền thì phản ứng xảy ra theo một chiều.
2. Este phản ứng thủy phân trong môi trường kiềm (phản ứng xà phòng hóa)
RCOOR’ + NaOH → RCOONa + R’OH
– mchất rắn sau phản ứng = mmuối + mkiềm dư.
– Với este đơn chức: neste phản ứng = nNaOH phản ứng = nmuối = nancol.
3. Một số phản ứng riêng của Este
– Este của ancol không bền khi thủy phân hoặc xà phòng hóa không thu được ancol:
RCOOCH=CH2 + H2O → RCOOH + CH3CHO
– Este của phenol phản ứng tạo ra hai muối và nước:
RCOOC6H5 + 2NaOH → RCOONa + C6H5ONa + H2O
– Este của axit fomic (HCOO)xR có khả năng tham gia phản ứng tráng gương.
(HCOO)xR + 2xAgNO3 + 3xNH3 + xH2O → (NH4CO3)xR + 2xAg + 2xNH4NO3
– Nếu este có gốc axit hoặc gốc Ancol không no thì este đó còn tham gia được phản ứng cộng, phản ứng trùng hợp và phản ứng oxi hóa không hoàn toàn.
CH2=CH-COOCH3 + Br2 → CH2Br-CHBr-COOCH3
nCH2=C(CH3)COOCH3 → (-CH2-C(CH3)(COOCH3)-)n
(Poli(MetylMetacrylat) – Plexiglass – thủy tinh hữu cơ)
nCH3COOCH=CH2 → (-CH2-CH(OOCCH3)-)n
(poli(vinyl axetat) – PVA)
V. Cách điều chế Este
1. Thực hiện phản ứng este hóa giữa ancol và axit
yR(COOH)x + xR’(OH)y 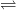 Ry(COO)xyR’x + xyH2O (H2SO4, t0)
Ry(COO)xyR’x + xyH2O (H2SO4, t0)
2. Thực hiện phản ứng cộng giữa axit và hiđrocacbon không no
RCOOH + C2H2 → RCOOCH = CH2
3. Thực hiện phản ứng giữa muối Na của axit và dẫn xuất halogen
RCOONa + R’X → RCOOR’ + NaX (xt, t0)
4. Thực hiện phản ứng giữa phenol và anhidrit axit
(RCO)2O + C6H5OH → RCOOC6H5 + RCOOH
VI. Ứng dụng của Este
* Các este có ứng dụng rộng rãi trong đời sống.
– Làm dung môi như: butyl và amyl axetat được dùng để pha sơn tổng hợp.
– Sản xuất nhiều chất quan trọng như: poli(metyl acrylat) và poli(metyl metacrylat) dùng làm thủy tinh hữu cơ; poli(vinyl axetat) dùng làm chất dẻo hoặc thủy phân thành poli(vinyl ancol) dùng làm keo dán.
– Một số este của axit phtalic được dùng là chất hóa dẻo, dược phẩm,…
– Một số este có mùi thơm hoa quả được dùng trong công nghiệp thực phẩm và mĩ phẩm,…
Ví dụ: Isoamyl axetat: CH3COOCH2CH2(CH3)2: mùi chuối, dùng trong thực phẩm
Geranyl axetat: CH3COOC10H17: mùi hoa hồng, dùng trong mỹ phẩm,…
VII. Cách nhận biết este
– Este của axit fomic có khả năng tráng gương.
– Các este của ancol không bền bị thủy phân tạo anđehit có khả năng tráng gương.
– Este không no có phản ứng làm mất màu dung dịch Brom
– Este của glixerol hoặc chất béo khi thủy phân cho sản phẩm hòa tan Cu(OH)2.
VIII. Bài tập về Este
Bài 2 trang 7 sgk hoá 12: Ứng với công thức C4H8O2 có bao nhiêu este là đồng phân của nhau?
A.2 B.3 C.4 D.5
* Lời giải bài 2 trang 7 sgk hoá 12:
Đáp án: C
+ Các công thức este là đồng phân C4H8O2:
HCOOCH2-CH2-CH3: n-propyl fomiat
HCOOCH(CH3)(CH3): isopropyl fomiat
CH3COOCH2-CH3: Etyl axetat
CH3-CH2COOCH3: Metyl propionat
Bài 3 trang 7 sgk hóa 12: Chất X có CTPT C4H8O2. Khi X tác dụng với dung dịch NaOH sinh ra chất Y có công thức C2H3O2 Na. Công thức cấu tạo của X là:
A. HCOOC3H7 B. C2H5COOCH3
C. CH3COOC2H5 D. HCOOC3H5
* Lời giải bài 3 trang 7 sgk hóa 12:
Đáp án: C
+ Theo bài ra Y có CTPT C2H3O2Na ⇒ CTCT của Y là CH3COONa
Như vậy X là : CH3COOC2H5 (Etyl axetat)
Bài 4 trang 7 sgk hóa 12: Khi thủy phân este X có công thức phân tử C4H8O2 trong dung dịch NaOh thu được hỗn hợp 2 chất hữu cơ Y, Z trong đó Z có tỉ khối hơi so với H2 bằng 23. Tên của X là:
A. Etyl axetat B. Metyl axetat.
C. Metyl propionat D. Propyl fomat.
* Lời giải bài 4 trang 7 sgk hóa 12:
Đáp án: A
– Vì Z có tỉ khối hơi so với H2 nên suy ra Z có thể ở dạng hơi. Do đó, Z là rượu.
– Theo bài ra CTPT của este X có dạng CnH2nO2 nên X là este no đơn chức mạch hở. Do đó, Z là rượu no đơn chức. Ta gọi CTPT của Z là CmH2m + 2O
Theo bài ra, ta có: 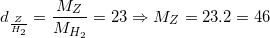
⇒ MZ = 14m + 18 = 46 ⇒ m = 2 ⇒ Z là C2H5OH (rượu etylic)
⇒ X là: CH3COOC2H5 (etyl axetat)
Bài 6 trang 7 sgk hóa 12: Đốt cháy hoàn toàn 7,4 gam este X đơn chức thu được 6,72 lít CO2 (đktc) và 5,4 gam nước.
a) Xác định công thức phân tử của X.
b) Đun 7,4 gam X trong dung dịch NaOH vừa đủ đến khi phản ứng hoàn toàn thu được 3,2 gam ancol Y và một lượng muối Z. Viết công thức cấu tạo của X và tính khối lượng của Z.
* Lời giải bài 6 trang 7 sgk hóa 12:
a) Ta có:
– Số mol CO2: nCO2= 6,72/22,4 = 0,3 (mol)
– Số mol nước là: nH2O = 5,4/18 = 0,3 (mol)
– Vì nCO2 = nH2O ⇒ X là este no đơn chức mạch hở. Gọi CTPT của este X là CnH2nO2
CnH2nO2 + 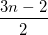 O2
O2 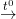 nCO2 + nH2O
nCO2 + nH2O
1 mol n mol
? mol 0,3 mol
– Theo PTPƯ: neste =0,3/n ⇒ Meste = 7,4/(0,3/n) = (74n)/3
⇔ 3(14n + 32) = 74n ⇒ n = 3
⇒ Công thức phân tử của este X là C3H6O2
b) Ta có: nx = m/M = 7,4/74 = 0,1 (mol).
– Ta gọi CTPT của X là RCOOR’, PTPƯ:
RCOOR‘ + NaOH → RCOONa + R‘OH
⇒ nR‘OH = nX = 0,1.
Y là rượu R‘OH, Z là muối RCOONa
Vì este X là no đơn chức nên Y cũng là rượu no đơn chức. Gọi CTPT của Y là CmH2m+2O
My = 3,2/0,1 = 32 ⇔ 14m + 18 = 32 ⇒ m = 1
⇒ Y là: CH3OH
Do đó este X là: CH3COOCH3 và muối Z là: CH3COONa.
nZ = 0,1 (mol) ⇒ mZ = 0,1.82 = 8,2 (g)
Công thức cấu tạo của X: 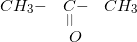
Bài 4 trang 18 sgk hóa 12: Làm bay hơi 7,4 gam một este A no, đơn chức thu được một thể tích hơi bằng thể tích của 3,2 gam khí oxi ở cùng điều kiện nhiệt độ và áp suất.
a) Tìm công thức phân tử của A.
b) Thực hiện phản ứng xà phòng hóa 7,4 gam A với dung dịch NaOH để phản ứng hoàn toàn thu được sản phẩm có 6,8 gam muối. Tìm công thức cấu tạo, gọi tên A.
* Lời giải bài 4 trang 18 sgk hóa 12:
a) Theo bài ra, số mol O2: nO2 = m/M = 3,2/32 = 0,1 (mol)
Vì A và O2 có cùng thể tích và ở cùng điều kiện nhiệt độ và áp suất nên nA = nO2 = 0,1 (mol)
⇒ MA = 7,4/0,1 = 74 g/mol.
Vì A là este no đơn chức nên có CTPT là CnH2nO2 (n ≥ 2)
Ta có: MCnH2nO2 = 12n + 2n + 32 = 74 ⇒ n = 3
⇒ CTPT của A là: C3H6O2
b) Gọi CTPT của A là RCOOR’ ta có PTPƯ xà phòng hoá
RCOOR‘ + NaOH 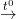 RCOONa + R‘OH
RCOONa + R‘OH
Theo PTPƯ: nRCOONa = nA = 0,1 mol
⇒ M(RCOONa) = 6,8/0,1 = 68 g/mol
M(RCOONa ) = MR + 12+32+23 = MR + 67 = 68 → R = 1
⇒ R là H (hay muối là HCOONa)
⇒ CTCT của A là: HCOOC2H5 (etyl fomat).
Bài 6 trang 18 sgk hóa 12: Khi thủy phân hoàn toàn 8,8 gam một este đơn chức mạch hở X với 100 ml dung dịch KOH 1M (vừa đủ) thu được 4,6 gam một ancol Y. Tên gọi của X là :
A. etyl fomiat. B. etyl propionat. C. etyl axetat. D. propyl axetat.
* Lời giải bài 6 trang 18 sgk hóa 12:
– Đáp án: C
– Gọi CTPT của este là RCOOR’
– Theo bài ra, số mol KOH: nKOH = V.CM = 0,1.1 = 0,1 (mol)
RCOOR’ + KOH 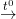 RCOOK + R’OH
RCOOK + R’OH
– Theo PTPƯ: nRCOOR1 = nKOH = 0,1 mol.
M(RCOOR’) = 8,8/0,1 = 88 g/mol
⇒ R + 44 + R’ = 88 (1)
M(R’OH) = 4,6/0,1 = 46 g/mol
⇒ R’ + 17 = 46 (2)
Từ (2) ⇒ R’ = 29 (C2H5-)
Thế vào (1) ⇒ R = 15 (CH3-)
⇒ Công thức cấu tạo là: CH3COOC2H5 (Etyl axetat)
Hy vọng với phần ôn tập và hệ thống lại tính chất hoá học của Este và bài tập về Este ở trên hữu ích cho các em, mọi thắc mắc các em hãy để lại bình luận dưới bài viết để Tmdl.edu.vn hỗ trợ, hãy like và chia sẻ cho bạn bè nếu thấy hay, chúc các em học tập tốt.
Bản quyền bài viết thuộc trường Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: Trường Tmdl.edu.vn (tmdl.edu.vn)
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục