Hoá 8 bài 20: Tỉ khối là gì, công thức và cách tính tỉ khối của chất khí, hỗn hợp khí. Khi học về tính chất của một chất khí nào đó, câu hỏi được đặt ra là làm thế nào để biết được chất khí đó nặng hay nhẹ hơn khí Oxi O2 , khí Hidro H2 , hay không khí.
Vậy tỉ khối của chất khí là gì? công thức tỉ khối của chất khí như thế nào? làm sao tính được tỉ khối của khí, hỗn hợp khí so với Hidro (H2) hay so với Oxi (O2), Heli (He) và không khí, tất cả sẽ được giải đáp qua bài viết này.
Bạn đang xem bài: Hoá 8 bài 20: Tỉ khối là gì, công thức và cách tính tỉ khối của chất khí, hỗn hợp khí
I. Tỉ khối của chất khí là gì?
• Khái niệm tỉ khối của chất khí:
– Tỉ khối là khái niệm chỉ sử dụng cho chất khí.
– Để biết khí A nặng hay nhẹ hơn khí B bao nhiêu lần, ta so sánh khối lượng mol của khí A (MA) với khối lượng mol của khí B (MB).
• Công thức tính tỉ khối của chất khí: 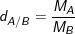
– Trong đó: 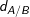 : tỉ khối của khí A đối với khí B
: tỉ khối của khí A đối với khí B
MA: khối lượng mol của khí A
MB: khối lượng mol của khí B
– Tỉ khối là công thức xác định phân tử khối của chất khí A so với chất khí B xem chất A nặng hay nhẹ hơn chất B bao nhiêu lần.
II. Khí A nặng hay nhẹ hơn khí B?
• Để biết khí A nặng hay nhẹ hơn khí B bao nhiêu lần, ta so sánh khối lượng mol của khí A với khối lượng mol của khí B.
– Công thức tính tỉ khối của khí A so với khí B: 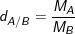
• Hoặc ngược lại, để biết khí B nặng hay nhẹ hơn A bao nhiêu lần, ta so sánh khối lượng mol của khí B so với khí A:
– Công thức tính tỉ khối của khí B so với khí A: 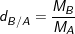
• Ví dụ: Muốn biết khí Oxi O2 nặng hay nhẹ hơn Hidro H2 bao nhiêu lần?
– Ta tính tỉ khối của Oxi (O2) so với Hidro (H2) : 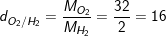
⇒ Vậy khí oxi nặng hơn khí hidro 16 lần.
III. Khí A nặng hay nhẹ hơn không khí?
• Thực tế, trong không khí là hỗn hợp nhiều khí, tuy nhiên, để đơn giản ta xem chứa 80% khí nito và 20% khí oxi. Khối lượng mol của không khí (tức là một mol không khí) được tính bằng khối lượng của 0,8 mol khí nito + 0,2 mol khí oxi:
Mkk = (28 x 0,8) + (32 x 0,2) ≈ 29 (g/mol).
• Vậy để biết khí A nặng hay nhẹ hơn không khí bao nhiêu lần ta so sánh khối lượng mol của khí A với khối lượng mol của không khí (=29g/mol)
– Công thức tính tỉ khối của khí A so với Không khí: 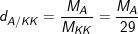
• Ví dụ: Khí hidro nhẹ hay nhẹ hơn không khí bao nhiêu lần?
– Ta tính tỉ khối của Hidro (H2) so với không khí:
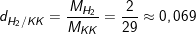
⇒ Vậy khí hidro nhẹ hơn không khí 0,069 lần (hay không khí nặng hơn khí hidro 14,49 lần).
IV. Cách tính tỉ khối của chất khí
1. Cách tính tỉ khối so với Hidro (H2).
– Tỉ khối của khí A so với Hidro (H2) tính theo công thức: 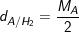
2. Cách tính tỉ khối so với Heli (He).
– Tỉ khối của khí A so với Heli (He) tính theo công thức: 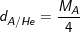
3. Cách tính tỉ khối so với Oxi (O2).
– Tỉ khối của khí A so với Oxi (O2) tính theo công thức: 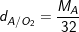
4. Cách tính tỉ khối so với Không khí.
– Tỉ khối của khí A so với không khí tính theo công thức: 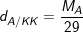
5. Cách tính tỉ khối của hỗn hợp khí
– Tỉ khối của HỖN HỢP khí A so với KHÍ B tính theo công thức: 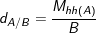
V. Bài tập áp dụng cách tính tỉ khối của chất khí
Bài 1 trang 69 SGK hoá 8: Có những khí sau: N2 , O2 ,Cl2 , CO , SO2.
Hãy cho biết:
a) Những khí nào nặng hay nhẹ hơn khí hiđro bao nhiêu lần?
b) Những khí nào nặng hơn hay nhẹ hơn không khí bao nhiêu lần?
* Lời giải bài 1 trang 69 SGK hoá 8:
a) Nhận xét : Trong số các khí thì khí hiđro là nhẹ nhất mH2= 2g vì vậy tất cả các khí đều nặng hơn khí hiđro. Ta có:
dN2/H2 = 28 : 2 = 14 lần.
dO2/H2 = 32 : 2 = 16 lần.
dCl2/H2 = 71 : 2 = 35,5 lần.
dCO/H2 = 28 : 2 = 14 lần.
dSO2/H2 = 64 : 2 = 32 lần.
b) dN2/kk = 28/29 ≈ 0,965 (Nitơ nhẹ hơn không khí và bằng 0,965 lần không khí)
dO2/kk = 32/29 ≈ 1,10 (Oxi nặng hơn không khí 1,103 lần)
dCl2/kk = 71/29 ≈ 2,448 (clo nặng hơn không khí 2,448 lần)
dCO/kk = 28/29 ≈ 0,965 (CO nhẹ hơn không khí và bằng 0,965 lần không khí)
dSO2/kk = 64/29 ≈ 2, 207 (SO2 nặng hơn không khí 2,207 lần).
Bài 2 trang 69 SGK hoá 8: Hãy tìm khối lượng mol của những khí:
a) Có tỉ khối đối với oxi là: 1,375 ; 0,0625.
b) Có tỉ khối đối với không khí là: 2,207; 1,172.
* Lời giải bài 2 trang 69 SGK hoá 8:
– Khối lượng mol của những khí cho:
a) 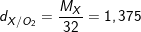 ⇒ Mx = 1,375.32 = 44(g/mol)
⇒ Mx = 1,375.32 = 44(g/mol)
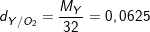 ⇒ MY = 0,0625.32= 2(g/mol)
⇒ MY = 0,0625.32= 2(g/mol)
b) 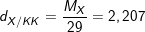 ⇒ Mx = 2,207.29 = 64(g/mol)
⇒ Mx = 2,207.29 = 64(g/mol)
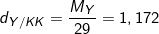 ⇒ MY = 1,172.29 = 34(g/mol)
⇒ MY = 1,172.29 = 34(g/mol)
Bài 3 trang 69 SGK hoá 8: Có thể thu những khí nào vào bình (từ những thí nghiệm trong phòng thí nghiệm) khí hiđro, khí clo, khí cacbon đioxit, khí metan bằng cách:
a) Đặt đứng bình.
b) Đặt ngược bình.
Giải thích việc làm này?
* Lời giải bài 3 trang 69 SGK hoá 8:
– Tính tỉ khối của từng khí hiđro, khí clo, khí cacbon đioxit, khí metan so với không khí, ta có:

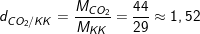
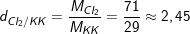
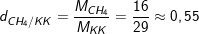
a) Đặt bình ngửa (miệng bình hướng lên trời) thu được những khí có tỉ khối đối với không khí lớn hơn 1
– Khí clo nặng hơn không khí 2,45 lần
– Khí cacbon đioxit nặng hơn không khí 1,52 lần
b) Đặt úp bình (miệng bình hướng xuống đất) thu được những khí còn lại có tỉ khối đối với không khí nhỏ hơn 1:
– Khí hiđro nhẹ hơn không khí và bằng 0,07 lần không khí
– Khí metan CH4 nhẹ hơn không khí và bằng 0,55 lần không khí.
Hy vọng với bài viết về tỉ khối khí, công thức và cách tính tỉ khối của chất khí, hỗn hợp khí so với Oxi, Hidro ở trên giúp ích cho các em. Mọi góp ý và thắc mắc các em vui lòng để lại bình luật dưới bài viết để Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá ghi nhận và hỗ trợ, chúc các em học tập tốt.
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn/hoa-8-bai-20-ti-khoi-la-gi-cong-thuc-va-cach-tinh-ti-khoi-cua-chat-khi-hon-hop-khi/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục