Hóa học 11 Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit – bazơ được Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá biên soạn hy vọng sẽ là là tài liệu hữu ích giúp các em nắm vững kiến thức bài học và đạt kết quả tốt trong các bài thi, bài kiểm tra trên lớp.
Tóm tắt lý thuyết Hóa học 11 Bài 3
Nước là chất điện li rất yếu
1. Sự điện li của nước
Bạn đang xem bài: Hóa học 11 Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit – bazơ – Giải bài tập SGK Hóa học 11 Bài 3
– Nước là chất điện li rất yếu. Thực nghiệm đã xác định được ở nhiệt độ thường cứ 555 triệu phân tử nước chỉ có 1 phân tử phân li ra ion.
– Phương trình điện li:
H2O⇄H++OH−H2O⇄H++OH-
2. Tích số ion của nước
– Ở 25oC, tích số KH2OKH2O= [H+].[OH–] được gọi là tích số ion của nước. Tích số này là hằng số ở nhiệt độ xác định. Tuy nhiên, giá trị tích số ion của nước thường được dùng trong các phép tính, khi nhiệt độ không khác nhiều so với 25oC.
KH2OKH2O = [H+].[OH–] = 10-14
⇒ [H+] = [OH–] = 10-7 M.
– Môi trường trung tính là môi trường trong đó:
[H+] = [OH–] = 10-7 M.
3. Ý nghĩa tích số ion của nước
a. Môi trường axit
– Là môi trường trong đó
[H+] > [OH–] hay [H+] > 10-7 M.
b. Môi trường kiềm
– Là môi trường trong đó
[H+] < [OH–] hay [H+] < 10-7 M.
Kết luận: Độ axit và độ kiềm của dung dịch có thể đánh giá bằng nồng độ H+.
+ Môi trường trung tính: [H+] = 10-7 M.
+ Môi trường axit: [H+] > 10-7 M.
+ Môi trường kiềm: [H+] < 10-7 M.
Khái niệm về pH. Chất chỉ thị axit – bazơ
1. Khái niệm về pH
– pH được dùng để đánh giá độ axit và độ kiềm của dung dịch.
– Quy ước: [H+]=1,0.10−pHMH+=1,0.10-pHM
Tức là: [H+]=1,0.10−aMH+=1,0.10-aM thì pH = a.
Về mặt toán học:
– Thang pH thường dùng có giá trị từ 1 đến 14, trong đó:
+ pH < 7: môi trường axit.
+ pH > 7: môi trường bazơ.
+ pH = 7: môi trường trung tính.
– Giá trị của pH có ý nghĩa to lớn trong thực tế. Chẳng hạn, pH của máu người và động vật có giá trị gần như không đổi hay tốc độ ăn mòn kim mòn kim loại trong nước tự nhiên phụ thuộc rất nhiều vào giá trị pH của nước.
2. Chất chỉ thị axit – bazơ
– Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
Ví dụ: Quỳ tím, phenolphatalenin.
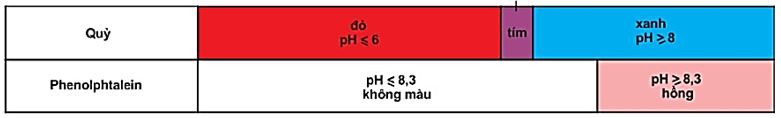
Hình 1: Màu của quỳ và phenolphtalein trong dung dịch ở các khoảng pH khác nhau
– Trộn lẫn một số chất chỉ thị có màu biến đổi kế tiếp nhau theo giá trị pH, ta được hỗn hợp chất chỉ thị vạn năng.
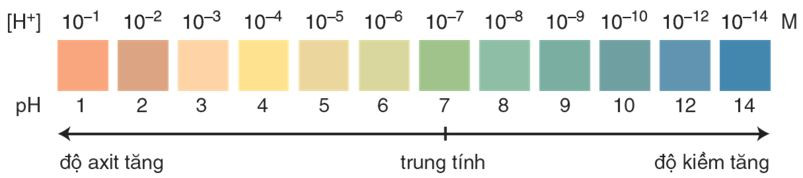
Hình 2: Màu của chất chỉ thị vạn năng (thuốc thử MERCK của Đức) ở các giá trị pH khác nhau
– Để xác định tương đối chính xác giá trị pH của dung dịch, người ta dùng máy đo pH.
3. Bảng công thức pH trong các môi trường

Giải bài tập SGK Hóa học 11 Bài 3
Bài 1 (trang 14 SGK Hóa 11)
Tích số ion của nước là gì và bằng bao nhiêu ở 25oC?
Lời giải:
Tích số ion của nước là tích số của nồng độ H+ và nồng độ OH– ([H+][OH– ] ) trong nước và cả trong các dung dịch loãng của các chất khác nhau. Ở 25oC bằng thực nghiệm, người ta xác định được [H+] = [OH–] = 10-7 (M).
Vậy tích số ion của nước (ở 25oC) là [H+][OH–] = 10-14.
Bài 2 (trang 14 SGK Hóa 11)
Phát biểu định nghĩa môi trường axit, trung tính và kiềm theo nồng độ H+ và pH?
Lời giải:
– Môi trường axit là môi trường trong đó [H+] > [OH–] hay [H+] > 10-7 M hoặc pH < 7.
– Môi trường trung tính là môi trường trong đó [H+] = [OH–] = 10-7 M hoặc pH = 7.
– Môi trường kiềm là môi trường trong đó [H+] < [OH–] hay [H+] < 10-7 MM hoặc pH > 7.
Bài 3 (trang 14 SGK Hóa 11)
Chất chỉ thị axit – bazơ là gì? Hãy cho biết màu của quỳ tím và phenolphtalein trong các khoảng pH khác nhau?
Lời giải:
Chất chỉ thị axit – bazơ là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
Màu của quỳ tím trong các khoảng pH khác nhau:
| pH | pH ≤ 6 | 6 < pH < 8 | pH ≥ 8 |
| Quỳ | Đỏ | Tím | Xanh |
Màu của phenolphtalien trong các khoảng pH khác nhau:
| pH | pH < 8,3 | 8,3 ≤ pH ≤ 10 |
| Phenolphtalien | Không màu | Hồng |
Bài 4 (trang 14 SGK Hóa 11)
Một dung dịch có [OH– ]= 1,5.10-5. Môi trường của dung dịch này là:
A. Axit ;
C. Kiềm
B. Trung tính ;
D. Không xác định được
Lời giải:
– Đáp án C
– Từ [OH–]= 1,5.10-5 (M) suy ra:
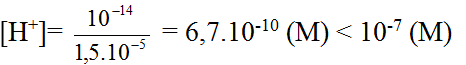
Vậy môi trường của dung dịch là kiềm.
Bài 5 (trang 14 SGK Hóa 11)
Tính nồng độ H+, OH– và pH của dung dịch HCl 0,10M và dung dịch NaOH 0,010M?
Lời giải:

Bài 6 (trang 14 SGK Hóa 11)
Dung dịch HCl 0,010M, tích số ion của nước là:
A. [H+][OH– ] > 1,0.10-14 ;
B. [H+ ][OH– ] = 1,0.10-14
C. [H+][OH– ] < 1,0.10-14 ;
D. Không xác định được
Lời giải:
– Đáp án B.
– Vì tích số ion của nước là hằng số trong nước và cả trong các dung dịch loãng của các chất khác nhau.
Trắc nghiệm Hóa học 11 Bài 3 có đáp án
Bài 1: Chọn câu trả lời đúng, khi nói về muối axit :
A. Dung dịch muối có pH < 7.
B. Muối cố khả năng phản ứng với bazơ.
C. Muối vẫn còn hiđro trong phân tử.
D. Muối mà gốc axit vẫn còn hiđro có khả năng phân li tạo proton trong nước.
Lời giải
Đáp án: D
Bài 2: Cho 10 ml dung dịch X chứa HCl 1M và H2SO4 0,5M. thể tích dung dịch NaOH 1M cần đẻ trung hòa dung dịch X là
A. 10 ml.
B. 15 ml.
C. 20 ml.
D. 25 ml.
Lời giải
Đáp án: C
H+ + OH– → H2O
Ta có: ⇒ V = 20 ml.
Bài 3: Dung dịch A có chứa 5 ion :Mg2+ ,Ba2+ ,Ca2+ và 0,1 mol Cl– và 0,2 mol NO3 . Thêm dần V ml dung dịch K2CO3 1M vào dung dịch A đến khi thu được lượng kết tủa lớn nhất. V có giá trị là
A. 150 ml.
B. 300 ml.
C. 200 ml.
D. 250 ml.
Lời giải
Đáp án: A
Khi thêm K2CO3 vào dung dịch A, khi lượng kết tủa thu được là lớn nhất tức là toàn bộ Mg2+, Ba2+, Ca2+ đã kết tủa, trong dung dịch còn lại KCl và KNO3
⇒ nK+ = nCl– + nNO3– = 0,3 mol
⇒ nK2CO3 = 0,15 mol
⇒ VK2CO3 = 150 ml
Bài 4: Trộn 200 ml dung dịch gồm HCl 0,1M vá H2SO4 0,15M với 300 ml dung dịch
Ba(OH)2 nồng độ aM, thu được m gam kết tủa và 500 ml dung dịch có pH = 1. Giá trị của a và m lần lượt là
A. 0,15 và 2,330
B. 0,10 và 6,990.
C.0,10 và 4,660
D. 0.05 và 3,495
Lời giải
Đáp án: D
Sau phản ứng trung hòa pH = 1 ⇒ H+ dư
H+ + OH– → H2O
nH+bd = 0,08 mol; sau phản ứng pH = 1
⇒ nH+ sau p/ư = 0,05 mol
nH+p/ư = nOH– = 0,03 mol
⇒ nBa(OH)2 = 0,015 mol
⇒ CM Ba(HCO3)2 = 0,05 (mol/l)
nBaSO4 = nBa(OH)2 = 0,015 mol (H2SO4 dư) ⇒ mBaSO4 = 3,495g
Bài 5: Cho 300 ml dung dịch chứa H2SO4 0,1M, HNO3 0,2M và HCl 0,3M tác dụng với V ml dung dịch NaOH 0,2 M và KOH 0,29M thu được dung dịch có pH = 2. Giá trị của V là
A. 134.
B. 147.
C. 114.
D. 169.
Lời giải
Đáp án: A
Coi 300 ml dung dịch A gồm 100 ml H2SO4 0,1M 100 ml HNO3 0,2M và 100 ml HCl 0,3M trộn lại với nhau. Vậy:
Phản ứng của dung dịch A và B là: H+ + OH– → H2O
nH+ p/ư = nOH– = 0,049.0,001V ⇒ nH+ p/ư = 0,01 (0,3 + 0,001V)
⇒ 0,07 = 0,49.0,001V + 0,010,3 + 0,001V) ⇒ V = 134 ml
Bài 6: Dung dịch có pH = 7 là:
A. NH4Cl.
B. CH3COONa.
C. C6H5ONa.
D. KClO3.
Lời giải
Đáp án: D
Bài 7: Khi hòa tan trong nước, chất nào sau đây làm cho quỳ tím chuyển màu xanh?
A. NaCl.
B. NH4Cl.
C. Na2CO3.
D. FeCl3.
Lời giải
Đáp án: C
Bài 8: Hãy cho biết dãy các dung dịch nào sau đây có khả năng đổi màu quỳ tím sang đỏ (hồng)?
A. CH3COOH, HCl và BaCl2.
B. NaOH, Na2CO3và Na2SO3.
C. H2SO4, NaHCO3và AlCl3.
D. NaHSO4, HCl và AlCl3.
Lời giải
Đáp án: D
Bài 9: Cho các dung dịch muối: Na2CO3 (1), NaNO3 (2), NaNO2 (3), NaCl (4), Na2SO4 (5), CH3COONa (6), NH4HSO4 (7), Na2S (8). Những dung dịch muối làm quỳ hoá xanh là:
A. (1), (2), (3), (4).
B. (1), (3), (5), (6).
C. (1), (3), (6), (8).
D. (2), (5), (6), (7).
Lời giải
Đáp án: C
(2) (4) (5): trung tính
(7): axit
Bài 10: Cho các muối sau đây: NaNO3; K2CO3; CuSO4; FeCl3; AlCl3; KCl. Các dung dịch có pH = 7 là :
A. NaNO3; KCl.
B. K2CO3; CuSO4; KCl.
C. CuSO4; FeCl3; AlCl3.
D. NaNO3; K2CO3; CuSO4.
Lời giải
Đáp án: A
K2CO3: Bazơ
CuSO4, FeCl3, FeCl2: Axit
Bài 11:Trộn V1 ml dung dịch NaOH có pH = 13 với V2 ml dung dịch Ba(OH)2 có pH = 11, thu được dung dịch mới có pH = 12. Tỉ số V1 : V2 có giá trị là
A. 1/1
B. 2/1
C. 1/10
D. 10/1
Lời giải
Đáp án: C
Ban đầu nOH– = 0,1. V1 + 0,002. V2
pH = 12 ⇒
⇒ V1 : V2 = 1/10
Bài 12: Trộn V1 lít dung dịch H2SO4 có pH = 3 với 2 lít dung dịch NaOH có pH = 12, thu được dung dịch mới cố pH = 4. Tỉ số V1 : V2 có giá trị là
A. 8/1
B. 101/9
C. 10/1
D. 4/1
Lời giải
Đáp án: B
Ban đầu nH+ = 0,001.V1; nOH– = 0,01.V2
Dung dịch sau có: pH = 4 ⇒
⇒ V1 : V2 = 101/9
Bài 13: Trộn hai dung dịch Ba(HCO3)2 và NaHSO4 có cùng nồng độ mol với nhau theo tỉ lệ thể tích 1 : 1 thu được kết tủa và dung dịch và dung dịch . Bỏ qua sự thủy phân của các ion và sự điện li của nước, các ion cos mặt trong dung dịch Y là
A. Na+và SO42-
B. Ba2+ ,HCO32- và Na+
C. Na+, HCO32-
D. Na+ , HCO32- và SO42-
Lời giải
Đáp án: C
Bài 14: Cho các dung dịch HCl, H2SO4 và CH3COOH có cùng giá trị pH. Sự sqps xếp nào sau đây đúng với giá trị nồng độ mol của các dung dịch trên?
A. HCl < H2SO4< CH3COOH
B. H2SO4< HCl < CH3COOH
C. H2SO4< CH3COOH < HCl
D. CH3COOH < HCl < H2SO4
Lời giải
Đáp án: B
Bài 15: Chỉ dùng quỳ tím , có thể nhận biết ba dung dịch riêng biệt nào sau đây?
A. HCl, NaNO3, Ba(OH)2
B. H2SO4, HCl,KOH.
C. H2SO4, NaOH, KOH
D. Ba(OH)2, NaCl, H2SO4
Lời giải
Đáp án: A
******************
Trên đây là nội dung bài học Hóa học 11 Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit – bazơ do Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá biên soạn bao gồm phần lý thuyết, giải bài tập và các câu hỏi trắc nghiệm có đáp án đầy đủ. Hy vọng các em sẽ nắm vững kiến thức về Sự điện li của nước. pH. Chất chỉ thị axit – bazơ. Chúc các em học tập thật tốt và luôn đạt điểm cao trong các bài thi bài kiểm tra trên lớp.
Biên soạn bởi: Trường Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá
Chuyên mục: Hoá học 11
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn https://tmdl.edu.vn/hoa-hoc-11-bai-23-su-dien-li-cua-nuoc-ph-chat-chi-thi-axit-bazo/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục





