Nguyên tắc chung để điều chế kim loại là gì? Có bao nhiêu phương pháp điều chế kim loại kiềm, kim loại hoạt động mạnh trong hóa học. Những câu hỏi này sẽ được giải thích chi tiết trong bài viết thuộc chủ đề hóa học này. hãy tham khảo ngay với Tmdl.edu.vnnhé !
Nguyên tắc điều chế kim loại chung
Dưới đây là hướng dẫn nguyên tắc chung được dùng để điều chế kim loại :
Bạn đang xem bài: Nguyên tắc điều chế kim loại là gì?
- Nguyên tắc chung để điều chế kim loại là : Trong tự nhiên, chỉ có một số ít kim loại như vàng, platin… tồn tại ở dạng tự do, hầu hết các kim loại còn lại đều tồn tại ở dạng hợp chất. Trong hợp chất, kim loại tồn tại dưới dạng ion dương Mn+
- Vì vậy, muốn điều chế kim loại ta phải khử ion kim loại thành nguyên tử.
Nên nguyên tắc điều chế kim loại là khử ion kim loại thành nguyên tử.
- Phương trình phản ứng tổng quát: Mn+ + ne -> M
- Nói một cách đơn giản là ta phải tách các hợp chất mà kim loại đó có thành nguyên tử kim loại độc lập.
Nguyên tắc chung để điều chế kim loại kiềm là gì? và phương pháp điều chế kim loại kiềm là gì ?
Vì sao phải điều chế kim loại : Vì các kim loại kiềm là một trong những chất khử mạnh nhất, nên việc điều chế kim loại kiềm ở dạng tinh khiết thì nguyên tắc chung để điều chế bất kỳ kim loại kiềm nào là sử dụng phương pháp điện phân nóng chảy. Có nghĩa là sử dụng một dòng điện mạnh để khử hợp chất và thu được kim loại kiềm nguyên chất.
Các phương pháp điều chế kim loại
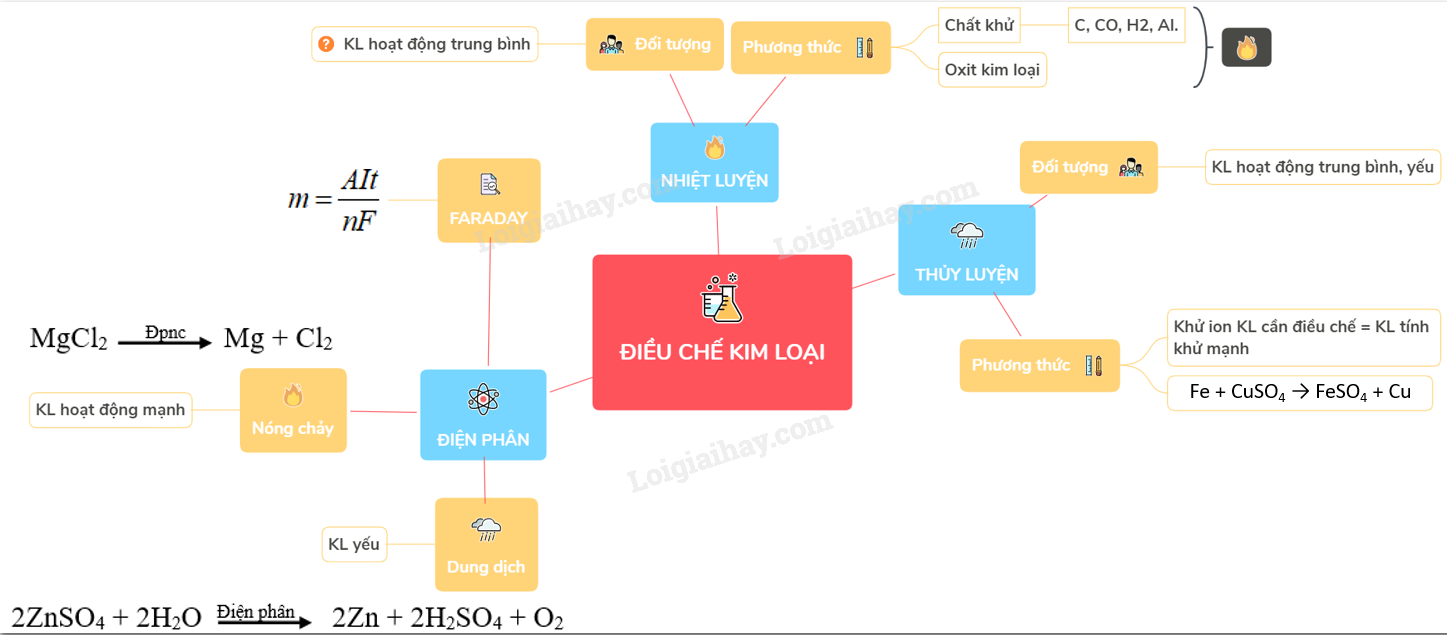
Có bạn thắc mắc có mấy phương pháp điều chế kim loại câu trả lời bên dưới nhé : Tùy thuộc vào độ hoạt động hóa học của kim loại mà người ta chọn phương pháp điều chế phù hợp, cụ thể gồm
Phương pháp nhiệt luyện
Những kim loại có độ hoạt động trung bình trong dãy điện hóa kim loại như Kẽm (Zn), Sắt (Fe), Thiếc ( Sn), Pb ( Chì ) … thường được điều chế bằng phương pháp nhiệt luyện, nghĩa là khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử như Cacbon ( C ), CO, Hidro (H2) hoặc các kim loại hoạt động mạnh hơn.
Ví dụ 1: cách điều chế kim loại bằng phương pháp nhiệt luyện
Fe2O3 + 3CO → 2Fe + 3CO2
ZnO + C → 2Zn + CO2
2ZnO + 2CO → 2Zn + 2CO2
PbO + H2 → Pb + H2O
Ví dụ 2: Cách điều chế Cu từ hợp chất Cu(OH)2
Phương trình phản ứng: Cu(OH)2 + H2 → Cu + 2H2O
Phương pháp nhiệt luyện được dùng để sản xuất kim loại trong công nghiệp. Chất khử thường được sử dụng trong công nghiệp là cacbon ( C ).
Phương pháp thủy luyện
Cơ sở của phương pháp này là dùng những dung dịch thích hợp như dung dịch H2SO4, NaOH, NaCl… để hòa tan kim loại hoặc hợp chất của kim loại và tách ra khỏi phần không tan có trong quặng. Sau đó khử những ion kim loại này trong dung dịch bằng kim loại có tính khử mạnh như Sắt (Fe), Kẽm (Zn)…
Ví dụ cách điều chế kim loại bằng phương pháp thủy luyện
Fe + CuSO4 → FeSO4 + Cu
Phương trình ion: Fe + Cu2+ → Fe2+ + Cu
Phương pháp điện phân dung dịch dùng để điều chế kim loại
Phương pháp điện phân có 2 cách gồm:
Điện phân hợp chất nóng chảy
Những kim loại hoạt động hóa học mạnh như Kali (K), Natri (Na), Canxi(Ca), Magie(Mg), Nhôm (Al) được điều chế bằng phương pháp điện phân nóng chảy các hợp chất của kim loại, nghĩa là khử ion kim loại bằng dòng điện.
Ví dụ 1: phương pháp điện phân để điều chế kim loại nhôm từ nhôm oxit
PTPƯ: 2Al2O3 → 4Al + 3O2
Ở catot ( cực âm ): Al3+ + 3e → Al
Ở anot ( cực dương): 2O2- → O2 + 4e
Phương pháp sản xuất nhôm trong công nghiệp phổ biến là sử dụng phương pháp điện phân nóng chảy Al2O3
Ví dụ 2: Cách điều chế kim loại Mg bằng điện phân nóng chảy
PTPƯ: MgCl2 → Mg + Cl2
Ở catot: Mg2+ + 2e → Mg
Ở anot: 2Cl– → Cl2 + 2e
Ví dụ 3: Cách điều chế Canxi (Ca) từ hợp chất CaCO3
PTPƯ: 2CaCO3 → 2Ca + 3CO2
Ví dụ 4: Cách điều chế Mg từ MgO
PTPƯ: 2MgO → 2Mg + O2
Điện phân dung dịch
Chúng ta cũng có thể điều chế nhiều kim loại hoạt động trung bình hoặc yếu bằng phương pháp điện phân dung dịch muối của chúng.
Ví dụ: Cách điều chế kim loại Đồng (Cu) bằng cách điện phân dung dịch CuCl2
PTPƯ: CuCl2 → Cu +Cl2
Ở catot: Cu2+ + 2e → Cu
Ở anot: 2Cl– → Cl2 + 2e
Cách tính lượng chất thu được ở các điện cực bằng phương pháp điện phân
Dựa theo công thức biểu diễn định luật Faraday, có thể xác định được khối lượng các chất thu được ở điện cực bằng công thức:
m = AIt / nF
Trong đó:
- m: Là khối lượng chất thu được ở điện cực ( đơn vị là gram)
- A: Là khối lượng mol nguyên tử của chất thu được ở điện cực.
- I: Là cường độ dòng điện ( đơn vị là ampe).
- t: Là thời gian điện phân ( tính bằng giây).
- n: Là số Electron mà nguyên tử hoặc ion đã cho hoặc nhận.
- F: Là hằng số Faraday, F = 96500
Trên đây là đáp án cho câu hỏi nguyên tắc điều chế kim loại là gì chi tiết và chính xác nhất. Cảm ơn bạn đã theo dõi bài viết.
Trang chủ: tmdl.edu.vn
Danh mục bài: Công thức Hóa Học




