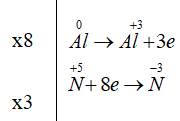Tổng hợp các công thức Hóa Học lớp 8
Chương trình Hóa học lớp 8 sẽ cung cấp hệ thống về các khái niệm cơ bản như chất, nguyên tử, phân tử, công thức hóa học, phương trính hóa học, số mol,… và hiểu biết sơ lược về bộ môn này. Sau chương trình Hóa học lớp 8 cần thành thạo tính toán số mol, công thức hóa học, viết phương trình hóa học, phân biệt được các chất cơ bản,…Dưới đây là các công thức hóa học lớp 8 quan trọng cần ghi nhớ.
Nội dung chính
Bạn đang xem bài: Tổng hợp các công thức Hóa Học lớp 8
Chương trình hóa học lớp 8
- Chương 1: Chất – Nguyên Tử – Phân tử
- Chương 2: Phản Ứng Hóa Học
- Chương 3: Mol Và Tính Toán Hóa Học
- Chương 4: Oxi – Không Khí
- Chương 5: Hiđro – Nước
- Chương 6: Dung Dịch
Công thức cơ bản theo chương
Chương I: Chất, nguyên tử, phân tử
Chương này chủ yếu cho các em hiểu khái niệm về chất, nguyên tử và phân tử là gì.
Chương II: Phản ứng hóa học
Định luật bảo toàn khối lượng:
mA + mB = mC + mD
Chương III: Mol và tính toán hóa học
Công thức tính số mol khi có khối lượng m (gam) :
n= mxM (mol)
Công thức tính số mol khi có thể tích V (l) chất khí:
n=Vx22,4 (mol)
Công thức tính tỉ khối của khí A đối với khí B:
d(A/B)=M(A)/M(B)
Tính thành phần phần trăm của nguyên tố X trong hợp chất Y:
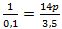
Chương IV: Oxi, không khí
Công thức tạo hợp chất oxit:
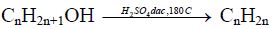
Chương V: Hidro, nước
Chương này chủ yếu giới thiệu về phản ứng oxi hóa-khử, tính chất hóa học của những chất axit, bazo, muối
Chương VI: Dung dịch
Công thức tính nồng độ phần trăm (C%) của một dung dịch cho ta biết số gam chất tan có trong 100g dung dịch:
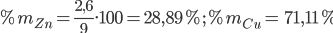
Trong đó:
- mct là khối lượng chất tan mdd là khối lượng dung dịch
- mdd = mct + mnước
Bài tập trắc nghiệm hóa 8 có lời giải
Câu 1: Nguyên tử có cấu tạo như thế nào?
A. Hạt nhân
B. Electron
C. Lớp vỏ
D.Chất
Câu 2: Câu nào dưới đây được biểu diễn bởi kí hiệu hóa học:
A.Phương trình hóa học
B.Phản ứng hóa học
C.Nguyên tố hóa học
D.Chất
Câu 3: Tìm hóa trị của Na trong các hợp chất sau đây gồm có Na2O, NaCl, NaOH là:
A. I.
B. II
C. III
D. IV.
Câu 4:Một mol của bất kì chất khí nào trong cùng đk to và ánh sáng đều chiếm thể tích là:
A. 2,24(lit)
B. 24(lit)
C. 22(lit)
D. 22,4(lit)
Câu 5: Oxi phản ứng được với các chất nào trong dãy chất dưới đây:
A. H2, Na, S
B. HCl, H2S, Fe
C. MgO, CuCl, H2
D. Cu, Na2O, KOH
Câu 6: Hiđrô là khí như thế nào?
A. Nhẹ nhất trong các loại khí.
C.Nặng hơn không khí
B.Nặng nhất trong các loại khí
D.Nặng hơn khí Oxi
Câu 7: Phân tử được tạo bởi 2 hay nhiều nguyên tử H2 liên kết với gốc axit gọi là:
A. Phân tử axit
C. Phân tử Oxit
B. Phân tử bazơ.
D. Phân tử muối.
Câu 8: Hoá trị của nhóm OH trong hợp chất Al (OH)3, Cu(OH)2, KOH là:
A. I
B. II
C. III
D. IV
Câu 9: Đốt 13g Cu trong Oxi sẽ thu được đồng oxit, m của oxi đã phản ứng là:
A. 6(g)
B. 7(g)
C. 0,7(g)
D. 17(g)
Câu 10: Cho sơ đồ phản ứng: Zn + 2HCl ZnCl + H2. Nếu có 0, 1 mol Zn tham gia phản ứng thì VH2 thu được là:
A. 22,4 (l)
B. 2,24(l)
C. 11,2 (l)
D. 1,12(l)
Câu 11: Cho sơ đồ phản ứng: C + O2 CO2. Nếu có 2lit oxi tham gia phản ứng thì VKK thu được sẽ là bao nhiêu?
A. 6(lit)
B. 7(lit)
C. 9(lit)
D. 10(lit)
Câu 12: Đốt Fe trong lọ đựng khí Oxi. Sản phẩm thu được là:
A. FeO
B. Fe2O3
C. Fe3O4
D. Fe3O2
Câu 13: Dãy chất nào trong các dãy chất sau đây là Axit:
A. H2SO4, SO2, Cu(OH)2
B. CO2, SO2, Na2O
C. HNO3, K2O, CuNO3.
D. H2O, MnO, Ca(OH)2
Câu 14: Phản ứng hoá học sau đây thuộc loại phản ứng hoá học nào: Cu + O2 CuO
A. Phản ứng hoá hợp
B.Phản ứng phân huỷ
C.Phản ứng thế
D. Phản ứng oxi hoá- khử
Câu 15: Cho Al vào H2SO4(l). Khí nào thu được sau phản ứng:
A. Oxi
B. Hiđrô
C.Cacbon đioxit
D. Clo
Câu 16: Các chất sau đây HNO3, H2O, HCl, NaOH đâu là Axít.
A: HNO3, HCl
B: HCl,NaOH
C: H2O, NaOH
D: H2O, HCl
Câu 17: Các chất sau đây: Cu(OH)2, HOH, C2H5OH, NaOH đâu là Bazơ.
A: HOH, Cu(OH)2
B: Cu(OH)2, NaOH
C: Cu(OH)2, C2H5OH
D: HOH, NaOH
Câu 18: Các chất sau đây: HCl, NaCl, H3PO4, K2CO3 đâu là muối:
A: NaCl, HCl
B: H3PO4, K2CO3
C: NaCl, K2CO3
D: H3PO4, NaCl
Câu 19: Hoà tan 15g đường vào nước. Cho biết C % của dung dịch thu được:
A: 30%
B: 35%
C: 25% D: 40%
Câu 20: Trong 200 ml dung dịch có hoà tan 16g Na2SO4, cho biết CM của dung dịch.
A. 1 Mol
B. 2 Mol
C. 0,5 Mol
D. 0,2 Mol
Câu 21: Công thức hoá học của hợp chất tạo bởi Ca (II) và NO3(I) là:
A. CaNO3
B. Ca2NO3
C. Ca2(NO3)3
D. Ca(NO3)2
Câu 22: Khối lượng của 0,1 mol Fe2O3 là:
A. 0,16(g)
B. 1,6(g)
C. 16(g)
D. 61(g)
Câu 23: 1, 5 mol Oxi có thể tích l à:
0,336(lit) B. 33,6(lit) C. 3,36(lit) D. 336(lit)
Câu 24: Thể tích của khí H2 và O2(đktc) cần tác dụng với nhau để tạo ra 1,8g H2O lần lượt là:
A. 2,24(l) H2 và 1,12(l) O2
B. 22,4(l) H2 và 11,2(l) O2
C. 0,24(l) H2 và 0,11(l) O2
D. 224(l) H2 và 11,2(l) O2
Trên đây là tổng hợp các công thức hóa học lớp 8 và một vài dạng bài tập cơ bản để giúp bạn hiểu hơn và nhớ công thức lâu hơn. Để tránh tình trạng mất căn bản môn hóa bạn cần phải học thuộc lòng và vận dụng nhanh những công thức cơ bản trên đây. Mong rằng bài viết này sẽ giúp ích cho bạn trong việc chinh phục môn Hóa học. Chúc các bạn học thật tốt và ghi có thể chinh phục được các câu bài tập trên.
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn/tong-hop-cac-cong-thuc-hoa-hoc-lop-8/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục