Zn + HNO3 → Zn(NO3)2 + N2O + N2 + H2O được Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá biên soạn hướng dẫn bạn đọc viết và cân bằng chính xác phản ứng Zn tác dụng HNO3 sản phẩm sinh ra 2 chất khử N2O và N2 (biết tỉ lệ mol của N2O : N2 = 2 : 3). Đây là dạng cân bằng phương trình oxi hóa khử khó, hy vọng thông qua tài liệu bạn đọc sẽ nắm được cách cân bằng cũng như biết cách vận dụng vào các dạng bài tập liên quan một cách tốt nhất. Mời các bạn tham khảo.
1. Phương trình phản ứng Zn tác dụng HNO3
23Zn + 56HNO3 → 23Zn(NO3)2 + 2N2O + 3N2 + 28H2O
2. Cân bằng phản ứng oxi hóa khử Zn + HNO3 → Zn(NO3)2 + N2O + N2 + H2O (biết tỉ lệ mol của N2O : N2 = 2 : 3)
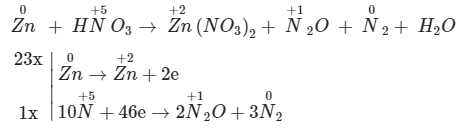
Bạn đang xem bài: Zn + HNO3 → Zn(NO3)2 + N2O + N2 + H2O
Vì tỉ lệ mol của N2O : N2 là 2 : 3
=> đặt 2 trước N2O và đặt 3 trước N2 sau đó tính tổng eletron nhận = 10.5 – 2.2.1 – 0 = 46
Chọn hệ số sao cho tổng electron cho = tổng electron nhận => nhân 23 ở quá trình cho eletron và nhân 1 ở quá trình nhận eletron
23Zn + 56HNO3 → 23Zn(NO3)2 + 2N2O + 3N2 + 28H2O
3. Điều kiện phản ứng Zn tác dụng HNO3
Nhiệt độ thường
4. Câu hỏi vận dụng liên quan
Câu 1. Cho 7,2 gam Mg tác dụng hết với dung dịch HNO3 (dư), sinh ra 4,48 lít khí X (sản phẩm khử duy nhất, ở đktc). Khí X là
A. N2O.
B. NO2.
C. N2.
D. NO.
Câu 2. Dung dịch Amoniac có thể hòa tan được Zn(OH)2 là do:
A. Zn(OH)2 là hidroxit lưỡng tính
B. Zn(OH)2 là một bazơ ít tan
C. Zn(OH)2 có khả năng tạo thành phức chất tan
D. Amoniac là một hợp chất có cực và là một bazơ yếu.
Câu 3. Hợp chất nào sau đây của nitơ không được tạo ra khi cho HNO3 tác dụng với kim loại?
A. N2O
B. NH4NO3
C. NO2
D. N2O5
Câu 4. Cho phản ứng aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O. Các hệ số a,b,c,d,e là những số nguyên đơn giản nhất. Tổng hệ số cân bằng tối giản trong phản ứng trên là
A. 8
B. 9
C. 7
D. 6
Phương trình hóa học
Fe + 4HNO3 → Fe(NO3)3 + NO↑ + 2H2O
Tổng hệ số cân bằng trong phản ứng = a + b + c + d + e = 1 + 4 + 1 + 1 + 2
Câu 5. Cho bột sắt vào dung dịch bạc natrat dư, sau khi kết thúc thí nghiệm thu được dung dịch X gồm:
A. Fe(NO3)2, H2O
B. Fe(NO3)2, AgNO3
C. Fe(NO3)2, AgNO3
D. Fe(NO3)2, Fe(NO3)3, AgNO3
…………………………
Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá đã gửi tới bạn Zn + HNO3 → Zn(NO3)2 + N2O + N2 + H2O được Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá biên soạn. Nội dung tài liệu giúp các bạn biết cách viết và cân bằng phương trình phản ứng oxi hóa khử Zn tác dụng với HNO3 cho 2 sản phẩm khử là N2O, N2 thay vì cho 1 sản phẩm khử duy nhất như các dạng phương trình trước đó. Từ nội dung tài liệu bạn đọc có thể biết cách vận dụng làm các dạng câu hỏi phương trình tương tự.
Các bạn có thể các em cùng tham khảo thêm một số tài liệu liên quan hữu ích trong quá trình học tập như: Giải bài tập Hóa 12, Giải bài tập Toán lớp 12, Giải bài tập Vật Lí 12 ,….
Ngoài ra, Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Tài liệu học tập lớp 12 Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.
Bản quyền bài viết thuộc Trường Trung Cấp Nghề Thương Mại Du Lịch Thanh Hoá. Mọi hành vi sao chép đều là gian lận!
Nguồn chia sẻ: https://tmdl.edu.vn/zn-hno3-znno32-n2o-n2-h2o/
Trang chủ: tmdl.edu.vn
Danh mục bài: Giáo dục